题目内容
 在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:
在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:N2O4(无色)?2NO2(红棕色)Q<0,隔一段时间对该容器内的物质进行分析得到如下数据:
时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)反应进行至100s后将反应混合物的温度降低,混合气体的颜色
(3)若要重新达到平衡时,使c(NO2)/c(N2O4)值变小,可采取的措施有(填序号)
A. 增大N2O4的起始浓度 B.向混合气体中通入NO2 C.使用高效催化剂 D.升高温度
(4)如果在80℃、将0.40mol的N2O4气体放入一个起始体积为2L、且压强维持不变的容器中发生上述反应.则达到平衡时n(NO2)
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线.
考点:化学平衡的影响因素,反应速率的定量表示方法,化学平衡建立的过程
专题:化学平衡专题
分析:(1)先根据二氧化氮物质的量计算20s内反应的四氧化二氮的物质的量,进而计算20s时容器内四氧化二氮的物质的量,再计算20s~40s参加反应的四氧化二氮的物质的量,再根据速率定义式计算四氧化二氮的平均反应速率;
(2)该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小;
(3)若使c(NO2)/c(N2O4)值变小,需使平衡向逆反应方向移动;
(4)压强不变则比原平衡的压强大,平衡向生成四氧化二氮的方向移动,使压强减小;
(5)降低温度,化学反应速率减小,平衡向放热方向移动.
(2)该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小;
(3)若使c(NO2)/c(N2O4)值变小,需使平衡向逆反应方向移动;
(4)压强不变则比原平衡的压强大,平衡向生成四氧化二氮的方向移动,使压强减小;
(5)降低温度,化学反应速率减小,平衡向放热方向移动.
解答:
解:(1)20s时△n(NO2)=0.24mol,故△n(N2O4)=
△n(NO2)=
×0.24mol=0.12mol,所以a=0.4mol-0.12mol=0.28mol,故20s~40s参加反应的四氧化二氮的物质的量为0.28mol-0.2mol=0.08mol,所以20s-40s内用N2O4表示的平均反应速率为
=0.002mol/(L?S),
故答案为:0.002mol/(L?S);
(2)该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小,气体的颜色变浅,
故答案为:变浅;
(3)若使c(NO2)/c(N2O4)值变小,需使平衡向逆反应方向移动,
A、增大N2O4的起始浓度,按勒夏特列原理,平衡移动的结果只能减弱这种改变,不能消除,所以,c(NO2)/c(N2O4)值变小,故A正确;
B、向混合气体中通入NO2 时,因为同时增大了体系的压强,平衡移动的结果,会使c(NO2)/c(N2O4)值变小,故B正确;
C、催化剂只能加快化学反应速率,不会影响平衡移动,故C错误;
D、升高温度会使平衡向生成二氧化氮的方向移动,会使c(NO2)/c(N2O4)值变大,故D错误;
故选:AB;
(4)压强不变则比原平衡的压强小,平衡向体积增大的方向移动,即向生成二氧化氮的方向移动,所以,n(NO2)增大,
故答案为:大于;
(5)当降低温度,化学反应速率减小,到达平衡所需时间增大,平衡向逆反应方向移动,所以到达新平衡时四氧化二氮的物质的量比第一次平衡时少,60℃曲线为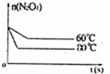 .
.
故答案为:
| 1 |
| 2 |
| 1 |
| 2 |
| ||
| 20s |
故答案为:0.002mol/(L?S);
(2)该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小,气体的颜色变浅,
故答案为:变浅;
(3)若使c(NO2)/c(N2O4)值变小,需使平衡向逆反应方向移动,
A、增大N2O4的起始浓度,按勒夏特列原理,平衡移动的结果只能减弱这种改变,不能消除,所以,c(NO2)/c(N2O4)值变小,故A正确;
B、向混合气体中通入NO2 时,因为同时增大了体系的压强,平衡移动的结果,会使c(NO2)/c(N2O4)值变小,故B正确;
C、催化剂只能加快化学反应速率,不会影响平衡移动,故C错误;
D、升高温度会使平衡向生成二氧化氮的方向移动,会使c(NO2)/c(N2O4)值变大,故D错误;
故选:AB;
(4)压强不变则比原平衡的压强小,平衡向体积增大的方向移动,即向生成二氧化氮的方向移动,所以,n(NO2)增大,
故答案为:大于;
(5)当降低温度,化学反应速率减小,到达平衡所需时间增大,平衡向逆反应方向移动,所以到达新平衡时四氧化二氮的物质的量比第一次平衡时少,60℃曲线为
 .
.故答案为:

点评:本题考查了化学反应速率、平衡移动、外界条件对化学平衡的影响图象,题目难度不大.

练习册系列答案
相关题目
(双项)下列物质的分子中所有的原子都在同一平面上的是( )
| A、氯乙烯 | B、乙烷 | C、甲烷 | D、乙烯 |
下列各组原子序数表示的两种元素中,能够形成共价化合物的是( )
| A、11与17 | B、11与10 |
| C、1与17 | D、1与8 |
既可以使溴水褪色,又可以使酸性高锰酸钾溶液褪色的气体有( )
| A、CH4 |
| B、CO2 |
| C、C2H4 |
| D、C2H6 |
 SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02mg/L.
SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02mg/L.