题目内容
【题目】能正确表示下列反应的离子方程式为
A. 硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S![]()
B. NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O
C. 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O=C6H5OH+HSO3-
D. 大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2![]() +H2O
+H2O
【答案】D
【解析】
A、硝酸具有氧化性,能氧化FeS,因此产物应该是硝酸铁、硫酸和一氧化氮,故A错误; B、NH4 HCO3 溶于过量的NaOH溶液中除了生成碳酸钠外还有氨气生成,方程式为NH 4 + +HCO3 - +2OH- =CO3 2-+2H2O+NH3 ↑,故B错误; C、HSO3 -的酸性比苯酚的强SO 2 不足产物应该是SO 3 2- ,少量SO 2 通入苯酚钠溶液中的离子反应为2C 6 H 5 O - +SO 2 +H 2 O=2C 6 H 5OH+SO 3 2- ,故C错误; D.碳酸钙和醋酸在离子反应中应保留化学式,大理石溶于醋酸中的离子反应为CaCO 3 +2CH 3 COOH=Ca 2+ +2CH 3COO - +CO 2 ↑+H 2 O,故D正确;故选D。

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
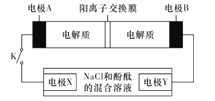
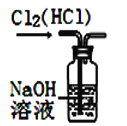
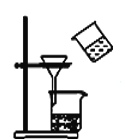
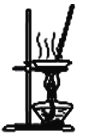
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
|
|
A.用CCl4提取溴水中的Br2 | B.从KI和I2的固体混合物中回收I2 |
|
|
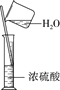
C.稀释浓硫酸 | D.工业酒精制备无水酒精 |
A. A B. B C. C D. D