题目内容
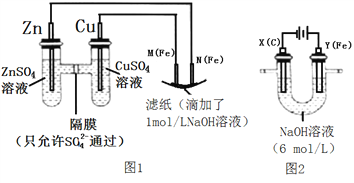
【题目】利用电化学原理将有机废水中的乙二胺[H2N(CH2)2NH2]转化为无毒物质的原理示意图如下图1所示,同时利用该装置再实现镀铜工艺示意图如图2所示,当电池工作时,下列说法正确的是

A. 图1中H+透过质子交换膜由右向左移动
B. 工作一段时间后,图2中CuSO4溶液浓度减小
C. 当Y电极消耗0.5 mol O2时,铁电极增重64 g
D. X 电极反应式:H2N(CH2)2NH2+16e-+4H2O═2CO2↑+N2↑+16H+
【答案】C
【解析】图1是原电池,Y电极上氧气被还原成水,所以Y是正极,氢离子移向正极,H+透过质子交换膜由左向右移动,故A错误;图2是电镀池,CuSO4溶液浓度不变,故B错误;当Y电极消耗0.5 mol O2时,转移电子2mol,根据电子数,铁电极生成1mol铜,电极增重64 g,故C正确;X是负极,失电子发生氧化反应,电极反应式是![]() ,故D错误。
,故D错误。

练习册系列答案
相关题目