题目内容
较活泼的金属锌与不同浓度的HNO3反应时,可得到不同价态的还原产物。如果起反应的锌和HNO3的物质的量之比为4 ∶10,则HNO3的还原产物可能为( )
| A.NO2 | B.NO | C.N2O | D.NH4NO3 |
CD
根据电子得失总数相等,4 mol Zn失去8 mol电子生成4 mol Zn2+,如果HNO3的还原产物中有两个变价氮原子,每个氮原子得到4个电子,还原产物中氮元素的化合价为+5+(-4)=+1,可能是N2O。如果HNO3的还原产物中只有一个变价的氮原子,这个氮原子得到8个电子,还原产物中氮元素的化合价为+5+(-8)=-3,可能是NH4NO3。

练习册系列答案
相关题目
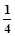 b mol
b mol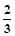 a mol
a mol 。
。 mol.L-1
mol.L-1 mol.L-1
mol.L-1 mol.L-1
mol.L-1 mol.L-1
mol.L-1