题目内容
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液等五项操作.不正确的操作顺序是( )
| A、⑤④②①③ |
| B、④①②⑤③ |
| C、②⑤④①③ |
| D、⑤②④①③ |
考点:化学实验操作的先后顺序
专题:实验题
分析:根据钙离子用碳酸根离子沉淀,镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子进行分析.
解答:
解:钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀;镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都行,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,如果加反了,过量的钡离子就没法除去;离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,选项中B加过量Na2CO3溶液在加过量BaCl2溶液前,操作不正确,
故选B.
故选B.
点评:本题主要考查了在粗盐提纯中物质的除杂或净化操作,在解此类题时,首先要了解需要除去的是哪些离子,然后选择适当的试剂进行除杂,在除杂质时,要注意不引入新的杂质.除杂质的顺序是解答的关键,题目难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
下列物质属于有机物的是( )
| A、氰化钾 KCN |
| B、氰酸铵 NH4CNO |
| C、聚乙炔 (C2H2)n |
| D、碳化硅 SiC |
将一定量的甲烷完全燃烧,使所生成的气体依次通过装有足量无水CaCl2和NaOH的玻璃管.结果盛NaOH的玻璃管质量增加了1.1g,则原来甲烷在标准状况下的体积为( )
| A、2.24L |
| B、1.12L |
| C、0.56L |
| D、0.28L |
下列离子方程式书写正确的是( )
| A、碳酸氢镁溶液中加入过量氢氧化钠:Mg2++2HCO3-+2OH-=MgCO3↓+2H2O |
| B、碳酸钡溶于醋酸溶液:BaCO3+2H+=Ba2++CO2↑+H2O |
| C、次氯酸钙溶液中通入少量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
| D、氧化铁加入氢碘酸中:Fe2O3+6H+=2Fe3++3H2O |
下列说法正确的是( )
| A、H、D、T属于同位素,H2、D2、T2属于同素异形体 |
| B、氯水、氨水、王水是混合物,铁粉、漂白粉是纯净物 |
| C、HCl、NH3、BaSO4是电解质,CO2、Cl2、C2H5OH是非电解质 |
| D、风能、生物质能是可再生能源,煤、石油、天然气是不可再生能源 |
下列有关碳酸钠和碳酸氢钠的说法,不正确的是( )
| A、常温下在水中的溶解度:碳酸钠>碳酸氢钠 |
| B、热稳定性:碳酸钠<碳酸氢钠 |
| C、等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少 |
| D、等物质的量的碳酸和碳酸氢钠分别与足量的盐酸反应,两者产生二氧化碳一样多,但消耗的盐酸不一样多 |
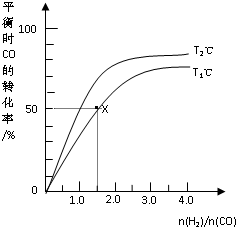 在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)?CH3OH(g)△H<0.有关信息如图所示,下列说法正确的是( )
在2L的密闭容器中,起始时均投入2mol CO,在不同条件下发生反应:CO(g)+2H2(g)?CH3OH(g)△H<0.有关信息如图所示,下列说法正确的是( )| A、T1<T2 | ||
| B、T1℃时该反应的平衡常数为4.0 L2?mol-2 | ||
C、同一温度下,
| ||
D、相同条件下
|