题目内容
【题目】某实验小组将SO2通入Na2S和Na2SO3的混合溶液中制备硫代硫酸钠(Na2S2O3)。其装置如下图所示(省略夹持装置),下列说法错误的是
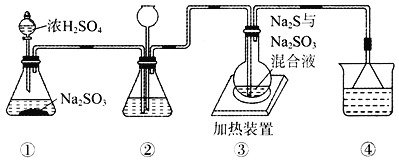
A. 装置②的作用之一是观察SO2的生成速率,其中的液体可以是饱和NaHSO3溶液
B. 为提高产品纯度,使烧瓶中Na2S和Na2SO3恰好完全反应,则![]()
C. 装置④的作用是吸收尾气,同时防止倒吸
D. 装置①也可用于高锰酸钾与浓盐酸反应制备氯气
【答案】B
【解析】装置②中气泡产生的速率越快,说明SO2的生成速率越快;SO2难溶于NaHSO3溶液,故A正确;根据反应方程式2Na2S+Na2SO3+3SO2=3Na2S2O3,所以![]() ,故B错误;装置④中盛放适当的试剂可以吸收SO2气体,倒置的漏斗同时防止倒吸,故C正确;高锰酸钾与浓盐酸反应制备氯气,属于固体与液体常温下反应制备气体,故D正确。
,故B错误;装置④中盛放适当的试剂可以吸收SO2气体,倒置的漏斗同时防止倒吸,故C正确;高锰酸钾与浓盐酸反应制备氯气,属于固体与液体常温下反应制备气体,故D正确。

练习册系列答案
相关题目