题目内容
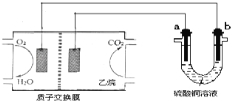
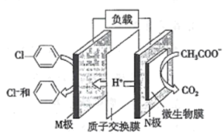
【题目】一种新型动力电池( LiFePO4电池)总反应式为Li1-xFePO4+LixC6![]() C6+LiFePO4,内部结构如图1所示,只有Li+通过聚合物隔膜。以此电池电解Na2SO4溶液(电极材料为石墨),可制得NaOH和H2SO4,其原理如图2所示。下列说法错误的是
C6+LiFePO4,内部结构如图1所示,只有Li+通过聚合物隔膜。以此电池电解Na2SO4溶液(电极材料为石墨),可制得NaOH和H2SO4,其原理如图2所示。下列说法错误的是

A. 电池放电时,LixC6在负极发生氧化反应
B. 电池放电时,正极反应式为 Lil-xFePO4+xLi-+xe-= LiFePO4
C. 电解时,图2的b电极反应式为2H2O-4e-=O2↑+4H+
D. 电解时,当转移0.2mol电子,A口产生气体的质量1.6g
【答案】D
【解析】
LiFePO4电池放电时,LixC6在负极上发生氧化反应,Li1-xFePO4在正极上发生还原反应。电解Na2SO4溶液可通过阴阳离子移向判断阴阳极。
A. 由电池的总反应可知,放电时, LixC6在负极上失电子发生氧化反应,A正确;
B.放电时,正极发生还原反应,电极反应式为Lil-xFePO4+xLi-+xe-= LiFePO4,B正确;
C.SO42-移向b极,说明b极为阳极,阳极发生失电子的氧化反应,电极反应为:2H2O-4e-=O2↑+4H+,C正确;
D.Na+移向a极,说明a极为阴极,阴极发生得电子的还原反应,电极反应为:2H2O+2e-=H2↑+2OH-,当转移0.2mol电子,产生氢气0.1mol,质量为0.2g;
答案:D。

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目