题目内容
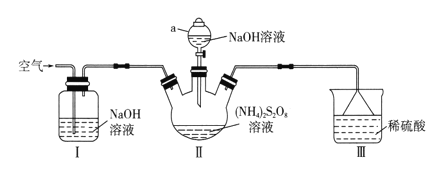
【题目】金属是重要但又匮乏的战略资源。从废旧锂电池的电极材料(主要为附在铝箔上的LiCoO2,还有少量铁的氧化物)中回收钴的一种工艺流程如下

请回答下列问题
(1)在焰色反应实验中,可用钴玻璃观察钾元素的焰色,该钴玻璃的颜色为_______。
(2)”溶液A中溶质除NaOH外,还有______。“钴渣”中LiCoO2溶解时的离子方程式为___________________________________。
(3)在“滤液”中加入20﹪Na2CO3溶液,目的是_________;检验“滤液1”中Fe2+是否完全被氧化、不能用酸性KMnO4溶液,原因是___________________________。
(4)如将硫酸改为盐酸浸取“钴渣“,也可得到Co2+。
①浸取时,为提高”钴渣”中浸取率,可采取的措施有_____________(任写一条)。
②工业生产中一般不用盐酸浸取“钴渣”,其原因是_____________________。
(5)”钴沉淀”的化学式可表示为CoCO3·yCo(OH)2。称取5.17g该样品置于硬质玻璃管中,在氮气中加热.使样品完全分解为CoO,生成的气体依次导入足量的浓硫酸和碱石灰中,二者分别增重0.54g和0.88g。则“钴沉淀”的化学式为__________。
【答案】蓝色 NaAlO2 或:偏铝酸钠 8LiCoO2+S2O32-+22H+==8Li++8Co2++2SO42-+11H2O 调节溶液pH,使Fe3+转换为Fe(OH)3沉淀 Co2+、S2O32-也能使KMnO4溶液褪色 粉碎;搅拌;升高温度 LiCoO2可氧化盐酸,产生的Cl2会污染环境 2CoCO3·3Co(OH)2
【解析】
(1)观察钾元素的焰色,黄色火焰会干扰,因此需要通过蓝色钴玻璃进行观察;
(2)电极材料中加入NaOH溶液,根据流程以及电极材料的成分,只有Al与NaOH溶液发生反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,溶液A中溶质除NaOH外,还有NaAlO2;Na2S2O3具有还原性,LiCoO2作氧化剂,Co被还原成Co2+,离子方程式为8LiCoO2+S2O32-+22H+=8Li++8Co2++2SO42-+11H2O;
(3)根据流程,滤液1中含有铁元素和锂元素等杂质,滤液2中除去Li+,则滤液1中加入NaClO3将Fe2+氧化成Fe3+,加入Na2CO3溶液,调节pH,使Fe3+转化成Fe(OH)3沉淀;“钴渣”操作步骤中加入Na2S2O3是过量,能使酸性高锰酸钾溶液褪色,同时滤液1中含有Co2+,也能使酸性高锰酸钾溶液褪色;
(4)①提高浸取率的采取措施有粉碎、搅拌、升高温度、适当提高硫酸的浓度等;
②Co3+的氧化性强于Cl2,用盐酸浸取,LiCoO2将盐酸中Cl元素氧化成Cl2,Cl2有毒,污染环境;
(5)根据题意,浓硫酸吸收产生H2O,即n(H2O)=0.54g/18g·mol-1=0.03mol,碱石灰的作用是吸收CO2,即n(CO2)=0.88g/44g·mol-1=0.02mol,因此有5.17g/M[CoCO3 ·yCo(OH)2]g·mol-1=0.02mol,解得y=3/2,即“钴沉淀”的化学式为2CoCO3·3Co(OH)2。