题目内容
2.下列表示物质或微粒的化学用语或模型正确的是( )| A. | N2的结构式:N-N | B. | Mg2+的结构示意图: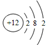 | ||
| C. | -CH3(甲基)的电子式: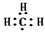 | D. | CO2分子的比例模型: |
分析 A.氮气分子中存在氮氮三键,不是单键;
B.镁离子的核外电子总数为10,最外层为8个电子;
C.甲基中含有3个碳氢键,碳原子最外层为7个电子;
D.二氧化碳分子中存在两个碳氧双键,碳原子相对体积应该大于氧原子.
解答 解:A.氮气分子中含有氮氮三键,氮气的电子式为 ,用短线代替所有共用电子对即为结构式,所以其结构式为N≡N,故A错误;
,用短线代替所有共用电子对即为结构式,所以其结构式为N≡N,故A错误;
B.镁离子的核电荷数为12,最外层为8个电子,镁离子的离子结构示意图为: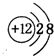 ,故B错误;
,故B错误;
C.甲基为中性原子团,碳原子最外层只有7个电子,-CH3(甲基)的电子式为: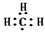 ,故C正确;
,故C正确;
D.二氧化碳为直线形结构,分子中存在两个碳氧双键,碳原子相对体积应该大于氧原子,二氧化碳正确的比例模型为: ,故D错误;
,故D错误;
故选C.
点评 本题考查了常见化学用语的判断,题目难度中等,试题涉及比例模型、离子结构示意图、结构式、电子式等知识,明确常见化学用语的表示方法为解答关键,试题培养了学生规范答题能力.

练习册系列答案
相关题目
12.下列分子式表示的物质一定是纯净物的是( )
| A. | CH2Cl2 | B. | C2H6O | C. | C3H6 | D. | C2H4Cl2 |
13.如表是元素周期表的一部分,根据所给的10 种元素,回答下列问题.
(1)金属性最强的元素是Na,最稳定的气态氢化物是HF(填化学式),适合制造半导体材料的元素是Si;
(2)表中所列第三周期的元素中,原子半径最小的是Cl,这些元素形成的简单离子中,离子半径最小的是Al3+(填离子符号);
(3)元素最高价氧化物对应的水化物中,酸性最强的是HClO4(填化学式),能证明Al(OH)3具有两性的实验是b(或bc、cd、bd)(填序号);
a.向AlCl3溶液中加入过量氨水
b.将铝条放入NaOH溶液中
c.向Al(OH)3浊液中滴入过量盐酸
d.向NaOH溶液中滴入少量AlCl3溶液
(4)举出能证明非金属性Cl>S的实验事实(举一例即可)氯气通入氢硫酸溶液中置换出硫.
| 周期 族 | I | II | III | IV | V | VI | VII | O |
| 二 | C | F | ||||||
| 三 | Na | Mg | Al | Si | S | Cl | Ar |
(2)表中所列第三周期的元素中,原子半径最小的是Cl,这些元素形成的简单离子中,离子半径最小的是Al3+(填离子符号);
(3)元素最高价氧化物对应的水化物中,酸性最强的是HClO4(填化学式),能证明Al(OH)3具有两性的实验是b(或bc、cd、bd)(填序号);
a.向AlCl3溶液中加入过量氨水
b.将铝条放入NaOH溶液中
c.向Al(OH)3浊液中滴入过量盐酸
d.向NaOH溶液中滴入少量AlCl3溶液
(4)举出能证明非金属性Cl>S的实验事实(举一例即可)氯气通入氢硫酸溶液中置换出硫.
10.有关化学用语正确的是( )
| A. | 乙醇的结构简式C2H6O | B. | 溴乙烷的分子式C2H5Br | ||
| C. | 羟基的电子式:${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$H | D. | 化学名词:苯、油酯、坩锅 |
7.下列说法中正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 水分子中氢原子之间不存在共价键 | |
| C. | 分子晶体中一定含共价键 | |
| D. | 阴、阳离子通过静电引力而形成的化学键叫离子键 |
14. 某有机物的结构如图所示,这种有机物可能具有的性质是( )
某有机物的结构如图所示,这种有机物可能具有的性质是( )
①能发生氧化反应;②能使溴水褪色;③能跟NaOH溶液反应;④能发生酯化反应;
⑤能发生加成反应;⑥能发生银镜反应.
 某有机物的结构如图所示,这种有机物可能具有的性质是( )
某有机物的结构如图所示,这种有机物可能具有的性质是( )①能发生氧化反应;②能使溴水褪色;③能跟NaOH溶液反应;④能发生酯化反应;
⑤能发生加成反应;⑥能发生银镜反应.
| A. | 只有②④ | B. | 只有②③④ | C. | 只有①②③④⑤ | D. | 全部 |
11.电解精炼粗铜时,下列叙述不正确的是( )
| A. | 与电源正极相连的电极是粗铜板 | B. | 阴极发生反应:Cu2++2e-═Cu | ||
| C. | 电解池的阳极材料为粗铜 | D. | 粗铜板上发生还原反应 |
12.下列说法正确的是( )
| A. | 浓硫酸能使蔗糖变黑,体现浓硫酸具有强酸化性 | |
| B. | 铵盐受热易分解,均有NH3产生 | |
| C. | 闪电时,N2转化为NO可以称为氮的固定 | |
| D. | 化工厂可通过加高烟囱排放废气,防止形成酸雨 |
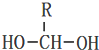 $\stackrel{-H_{2}O}{→}$
$\stackrel{-H_{2}O}{→}$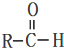
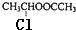 ,④的反应类型取代反应(或水解反应).
,④的反应类型取代反应(或水解反应).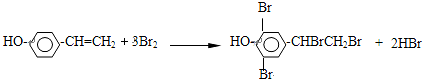 .
.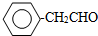 或
或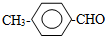 .
.