题目内容
【题目】以下有关描述正确的个数是( )
①甲苯分子中的所有原子可能共平面 ②苯乙烯![]() 中的所有原子可能共平面
中的所有原子可能共平面
③二氯甲烷分子为正四面体结构 ④乙烷分子中的所有原子不可能都在同一平面内
⑤甲烷分子中的4个氢原子全部被苯基取代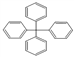 ,其分子内的所有碳原子可能共平面
,其分子内的所有碳原子可能共平面
A. 1 B. 2 C. 3 D. 4
【答案】B
【解析】①由于甲烷为正四面体结构,甲苯可以看作甲烷中1个H被苯基取代,所以甲苯中所有原子不可能共平面,故①错误;②苯和乙烯都是平面机构,所有原子共平面,则苯乙烯分子中所有原子可以共平面,故②正确;③二氯甲烷中存在两个C-Cl键和2个C-H键,由于它们的键长不同,所以二氯甲烷不可能为正四面体结构,故③错误;④乙烷中可以看作甲基取代了甲烷分子中的一个氢原子,甲烷为正四面体结构,则乙烷分子为四面体结构,分子中所有原子不可能共平面,故④正确;⑤由于甲烷为正四面体结构,甲烷分子中的4个氢原子全部被苯基取代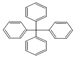 ,其分子内的所有碳原子不可能共平面,故⑤错误;正确的②④,故选B。
,其分子内的所有碳原子不可能共平面,故⑤错误;正确的②④,故选B。

【题目】马日夫盐[Mn(H2PO4)2·2H2O]是一种白色晶体,易溶于水,常用于机械设备的磷化处理。以软锰矿(主要成分为MnO2,还含有少量的Fe2O3、FeO和A l 2O3)为原料制备马日夫盐的流程如下:
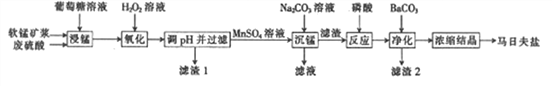
⑴软锰矿要先制成矿浆的目的是______________,葡萄糖(C4H12O6)与MnO2反应时,产物为MnSO4、CO2和H2O,该反应中氧化剂与还原剂的物质的量之比为___________________。
(2)用H2O2溶液“氧化”时发生反应的离子方程式为_______________________。
(3)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如下表,“调pH并过滤”时,应调整的pH范围为______________,滤渣1的主要成分为____________(填化学式)。
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.8 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
Mn2+ | 7.8 | 9.8 |
(4)加入磷酸后发生反应的化学方程式为_____________________。
(5)某工厂用上述流程制备马日夫盐,已知软锰矿中MnO2的含量为87%,整个流程中锰元素的损耗率为9% ,则1吨该软锰矿可制得马日夫盐________t。
【题目】化学反应原理在科研和生产中有广泛应用。
(1)已知:3Fe2O3(s)+CO(g)=2Fe3O4(s)+4CO2(g) △H1=-47kJ/mol;
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H2=-14kJ/mol。
则Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=________。
(2)煤化工行业中常常通过研究不同温度下反应的平衡常数来解决各种实际问题。将等体积的CO和H2O(g)通入一恒容密闭容器中,发生反应:CO(g)+H2O(g)![]() H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表所示。
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表所示。
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
① 该反应的平衡常数表达式K=_______,该反应的正反应是_______(填“吸热”或“放热”)反应。
② 若反应在800℃时进行, CO和H2O(g)的起始浓度均为0.020 mol·L-1,则该条件下,CO的平衡转化率为_________。
③ 下列措施中能够提高CO转化率的是______(填字母)
a.降低温度 b.加入催化剂 c.增加CO的浓度 d.加入H2O(g)