题目内容
3.下列反应的离子方程式正确的是( )| A. | 向Ca(ClO)2中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| B. | 醋酸与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 向AlCl3溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4+ | |
| D. | NO2与水的反应:3NO2+H2O═2NO3-+NO+2H+ |
分析 A.发生氧化还原反应生成硫酸钙;
B.醋酸在离子反应中保留化学式;
C.反应生成氢氧化铝和氯化铵;
D.反应生成硝酸和NO.
解答 解:A.向Ca(ClO)2中通入少量SO2的离子反应为SO2+H2O+Ca2++3ClO-═CaSO4↓+Cl-+2HClO,故A错误;
B.醋酸与水垢中的CaCO3反应的离子反应为CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑,故B错误;
C.向AlCl3溶液中加入过量的氨水的离子反应为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故C错误;
D.NO2与水的反应的离子反应为3NO2+H2O═2NO3-+NO+2H+,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应考查,注意电子、电荷守恒分析,题目难度不大.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
13.2014年是门捷列夫诞辰180周年,下列事实不能用元素周期律解释的有( )
| A. | 碱性:KOH>NaOH | B. | 溶解度:SO2>CO2 | ||
| C. | 酸性:HClO4>H2SO4 | D. | 气态氢化物的稳定性:H2O>NH3 |
14.下列现象中,不是因为发生化学反应而产生的是( )
| A. | 将苯滴入溴水中,振荡后水层接近无色 | |
| B. | 乙烯使酸性KMnO4溶液褪色 | |
| C. | 乙烯使溴的四氯化碳溶液褪色 | |
| D. | 甲烷与氯气混合,光照一段时间后黄绿色消失 |
18.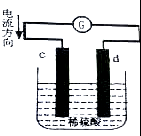 如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c,d为两个电极.则下列有关的判断不正确的是( )
如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c,d为两个电极.则下列有关的判断不正确的是( )
 如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c,d为两个电极.则下列有关的判断不正确的是( )
如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c,d为两个电极.则下列有关的判断不正确的是( )| A. | d为负极,电池工作时,d极发生氧化反应 | |
| B. | c为锌片,电池工作时,溶液中SO42-向c极移动 | |
| C. | 电池工作的过程中,d电极上产生大量的气泡 | |
| D. | 电池工作的过程中,溶液的pH基本不变 |
12.标准状况下,由甲烷和乙烯组成的混合气体,其密度为1g•L-1,则该混合气体中甲烷与乙烯的质量比为( )
| A. | 1:2 | B. | 2:1 | C. | 7:8 | D. | 8:7 |

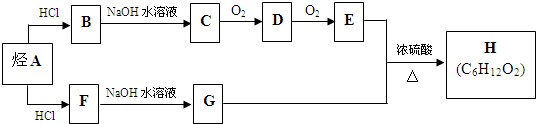

 .(用结构简式表示)
.(用结构简式表示) .
.