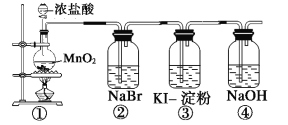
��Ŀ����
����Ŀ����������(Na2FeO4)���к�ǿ�������ԣ���һ�����͵���ɫ��ˮ����������ҵ����������(��Ҫ�ɷ���FeCO3������SiO2)Ϊԭ���Ʊ��������������������£�
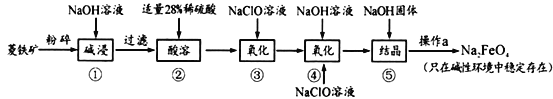
(1)Na2FeO4����Ԫ�صĻ��ϼ�Ϊ_____________��������������ɱ������ʱ�Ļ�ѧ��Ӧ����Ϊ_______________(����������ԭ��Ӧ���������ֽⷴӦ���������Ϸ�Ӧ��)��
(2)�����������̣�������м��ʱ�ܷ��ýϱ��˵�Ca(OH)2���NaOH___________ (������������������)��������________________________��
(3)������м���Fe2+ȫ��ת����Fe3+�ķ����ǣ�___________________________��
(4)������г�����Na2FeO4�⣬����NaCl���ɣ������ӷ���ʽΪ_____________����֪���������Na2FeO4��Һ�м��������������ƹ���õ�����Һ�������a������Ϊ_____��
(5)���������У�������ÿ���0.5mol��FeO42-���� NaClO��������Ϊ_______________��
(6)��֪����������20��ʱ��Ksp���±���
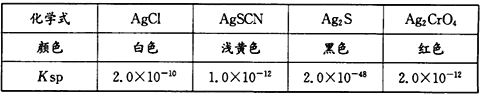
ijͬѧ�õζ����ⶨ����CoCl2��xH2O�е�x�����ñ������������еζ����ζ�ʱѡ���ָʾ����_____(����)��
A.KCl B.KSCN C.K2S D.K2CrO4
��ȡ������Ʒag��������ˮ������100mL��Һȡ20mL������Һ����ƿ�У�������ѡָʾ������cmol/LAgNO3��Һ�ζ����յ����ı���ҺbmL����x�ı���ʽΪ___________��
���𰸡�+6 ������ԭ��Ӧ ���� CaSiO3������ˮ���������SiO2 ȡ����������Һ���Թܣ��������� K3Fe(CN)6��Һ��������ɫ�������� Fe2+�Ѿ�ȫ��ת����Fe3+ 2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O ���� 74.5g D ![]()
��������
����������(��Ҫ�ɷ���FeCO3������SiO2)������NaOH��Һ���ܣ�����������SiO2��NaOH��Ӧ�õ���������Һ�����ˣ�������Ҫ����FeCO3������ϡ�����ܽ⣬�õ�Fe2+��������Һ������NaClO��Һ����Fe2+��2Fe2++ClO-+2H+=2Fe3++Cl-+H2O���ټ���NaOH��NaClO��Һ��������Fe3+����ӦΪ��2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O����õ���Na2FeO4��Һ�м��������������ƹ���õ�����Һ�����˵õ��������ƣ��ݴ˷������
(1)Na2FeO4����Ԫ��+1�ۣ���Ԫ��-2�ۣ�����Ԫ��+6�ۣ�������������Ԫ��+6�ۣ�����ǿ�����ԣ���ɱ���������ʷ���������ԭ��Ӧ��
(2)������Ca(OH)2���NaOH��Ca(OH)2����SiO2������Ӧ����CaSiO3��CaSiO3������ˮ���������SiO2��
(3)������м���Fe2+ȫ��ת����Fe3+�ǿ���Һ���Ƿ���Fe2+,����ȡ����������Һ���Թܣ�����������K3Fe(CN)6��Һ��������ɫ��������Fe2+ȫ��ת����Fe3+��������Fe2+��
(4)�����ΪNaOH��NaClO��Һ����Fe3+����Na2FeO4��NaCl�����ݵ����غ㡢����غ㼰ԭ���غ㣬�ɵø÷�Ӧ�����ӷ���ʽ��2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O�����������Na2FeO4��Һ�м��������������ƹ���õ�����Һ����������a�õ����壬��÷�������IJ�������Ϊ���ˣ�
(5)������Ԫ���غ㣬����0.5mol��FeO42-��������Fe2+Ϊ0.5mol����һ�μ���NaClO��Һ����Fe2+��������Ӧ2Fe2++ClO-+2H+=2Fe3++Cl-+H2O������Ҫn(NaClO)=0.25mol���ڶ��μ���NaOH��NaClO��Һ��������Fe3+��������Ӧ2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O������Ҫn(NaClO)=0.75mol���������� NaClO��������Ϊm(NaClO)=(0.25mol+0.75mol)��74.5g/mol=74.5g��
(6)ָʾ����������ָʾCl-ǡ�ó�����ȫ����ʹCl-���γɳ������ٵ���AgNO3��Һʱ������ͬ��ɫ�ij�����ָʾ�ζ��յ㡣
A.KCl����AgCl��ɫ������û�����Ե���ɫ�仯��A����
B.���ݱ������ݿ�֪AgSCN���ܽ�ȱ�AgClС�����γ�AgSCN������B����
C.Ksp(Ag2S)=2.0��10-48=c2(Ag+)��c(S2-)��c(S2-)=![]() mol/L��Ksp(AgCl)= c(Ag+)��c(Cl-)=2.0��10-10��c(Cl-)=
mol/L��Ksp(AgCl)= c(Ag+)��c(Cl-)=2.0��10-10��c(Cl-)=![]() mol/L��˵��Ag2S���ܽ��С��AgCl���ܽ�ȣ��μ�ʱ���γ�Ag2S������C����
mol/L��˵��Ag2S���ܽ��С��AgCl���ܽ�ȣ��μ�ʱ���γ�Ag2S������C����
D.Ksp(Ag2CrO4)= c2(Ag+)��c(CrO42-)=2.0��10-12��c(CrO42-)=![]() mol/L>
mol/L>![]() mol/L��˵��Ag2CrO4���ܽ�ȴ���AgCl���ܽ�ȣ������K2CrO4������ָʾ����ָʾ�ζ��յ㣬D��ȷ���ʺ���ѡ����D��
mol/L��˵��Ag2CrO4���ܽ�ȴ���AgCl���ܽ�ȣ������K2CrO4������ָʾ����ָʾ�ζ��յ㣬D��ȷ���ʺ���ѡ����D��
ag������Ʒ�к���Cl-�����ʵ���Ϊn(Cl-)=n(Ag+)=cmol/L��b��10-3L��![]() =5bc��10-3mol��n(CoCl2)=
=5bc��10-3mol��n(CoCl2)=![]() n(Cl-)=
n(Cl-)=![]() 5bc��10-3mol=2.5bc��10-3mol�������ɵ�x�ı���ʽΪ
5bc��10-3mol=2.5bc��10-3mol�������ɵ�x�ı���ʽΪ![]() ��
��

 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�����Ŀ������ʵ���о��к���ɫ����������Աȷ������ý��۲���ȷ���ǣ� ��
|
|
|
�� | �� | �� |
A.�ɢ��еĺ���ɫ���壬�ƶϲ���������һ���ǻ������
B.����ɫ���岻�ܱ�������ľ̿��Ũ���ᷢ���˷�Ӧ
C.�ɢ�˵��Ũ������лӷ��ԣ����ɵĺ���ɫ����Ϊ��ԭ����
D.�۵���������м���CO2���ɴ�˵��ľ̿һ����Ũ���ᷢ���˷�Ӧ
����Ŀ����X��Һ�л����μ�Y��Һ�����ɳ�����������ͼ��ʾ������ͼ���һ����

X | Y | |
A | AlCl3��Mg(NO3)2��HNO3 | NaOH |
B | Na2CO3��NH4HCO3��Na2SO4 | Ba(OH)2 |
C | NH4NO3��Al(NO3)3��Fe(NO3)3��HCl | NaOH |
D | NaAlO2����ˮ��NaOH | H2SO4 |