题目内容
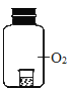
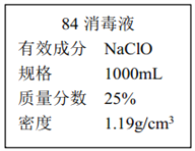
【题目】资料显示“O2 的氧化性随溶液pH的增大逐渐减弱”。某兴趣小组探究不同条件下KI与O2的反应。实验如下:
装置 | 烧杯中的液体 | 现象(5分钟后) |
| ①2mL1mol/LKI溶液+5滴淀粉 | 无明显变化 |
②2mL1mol/LKI 溶液+5滴淀粉+1mL0.1mol/L HCl | 溶液变蓝 | |
③2mL1mol/LKI溶液+5 滴淀粉+1mL0.1mol/L KCl | 无明显变化 | |
④2mL1mol/LKI溶液+5滴淀粉+1mL0.1mol/L CH3COOH | 溶液变蓝,颜色较②浅 |
下列说法不正确的是
A. 通过小烧杯中溶液颜色的变化证明反应的发生
B. ③是验证Cl-是否影响KI与O2的反应
C. ④说明CH3COOH 是弱酸,因为和盐酸同浓度同温度的情况下,电离出 c(H+)浓度低
D. 此实验还可以增加2mL1mol/LKI溶液+5 滴淀粉+1mL0.1mol·L-1NaOH 溶液这一步骤
【答案】D
【解析】A. 溶液变蓝,说明生成碘单质,反应的离子的方程式为:4I-+O2+4H+=2I2+2H2O,可以通过小烧杯中溶液颜色的变化证明反应的发生,故A正确;B. 根据实验2和实验3的所加试剂的区别可知,实验3是对照实验,验证Cl-是否影响KI与O2的反应,故B正确;C. 盐酸是强电解,而醋酸是弱电解质,同浓度的两种酸氢离子浓度不同,所以其他条件相同时,CH3COOH是弱电解质,溶液中c(H+)较盐酸小,O2的氧化性减弱,故C正确;D.即使生成了碘单质,碘单质能够迅速与氢氧化钠溶液反应,也看不到明显的现象,因此没有必要增加2mL1mol/LKI溶液+5 滴淀粉+1mL0.1mol·L-1NaOH 溶液这一步骤,故D错误;故选D。

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案【题目】羰基硫(COS)常用作粮食熏蒸剂,制取反应为 CO(g)+H2S(g) ![]() COS(g)+H2(g),△H=-30kJ·mol-1。在恒容的密闭容器中不同条件下发生反应并达到平衡,数据如下表。
COS(g)+H2(g),△H=-30kJ·mol-1。在恒容的密闭容器中不同条件下发生反应并达到平衡,数据如下表。
实验 | 温度/℃ | n起始/mol | 平衡时 | 所需时间 | |||
CO | H2S | COS | H2 | n(CO)/mol | min | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 | e |
2 | 150 | 7.0 | 7.0 | 3.0 | 3.0 | a | f |
3 | 200 | 20.0 | 20.0 | 0 | 0 | 16.0 | g |
下列说法错误的是
A. 实验1 反应开始到平衡整个过程中放出的热量为 90kJ
B. 实验2 达平衡时,a>7.0
C. 实验3 时间:g<e
D. 实验3 CO 达到平衡时的转化率比实验1 小