题目内容
12.下列关于元素周期表和元素周期律的说法错误的是( )| A. | Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多 | |
| B. | 第二周期元素从Li到F,非金属性逐渐增强 | |
| C. | 因为Al比Mg失去电子数多,所以Al比Mg的还原性强 | |
| D. | O与S为同主族元素,且O比S的非金属性强 |
分析 同周期元素的原子从左到右,元素非金属性逐渐增强;同周期元素的原子从左到右,元素非金属性逐渐增强,失电子能力逐渐减弱.
解答 解:A、Li、Na、K属同一主族,核外电子层数随着核电荷数增加而增多,故A正确;
B、根据元素周期律:同周期元素的原子从左到右,元素非金属性逐渐增强,可推知第二周期元素从Li到F非金属性逐渐增强,故B正确;
C、Al与Mg比较,Mg更易失电子,还原性更强,故C错误;
D、同主族元素的原子从上到下,元素非金属性逐渐减弱,O与S同主族,O的非金属性强,故D正确.
故选C.
点评 本题主要考查学生元素周期律的知识,可以根据所学知识来回答,难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
20.下列表示对应的离子方程式正确的是( )
| A. | 纯碱与醋酸反应:CO32-+2H+=H2O+CO2↑ | |
| B. | 等物质的量的SO2和Cl2通入水中:SO2+Cl2+2H2O=4H++SO42-+2Cl- | |
| C. | NH4HCO3溶液与过量的浓NaOH溶液反应:NH4++OH-=NH3↑+H2O | |
| D. | 锌与稀硝酸反应:Zn+2H+=Zn2++H2↑ |
7.足量的锌加入100mL18mol/L的浓硫酸中充分反应,则被还原的H2SO4的物质的量为( )
| A. | 1.8mol | B. | <0.9mol | ||
| C. | 0.9mol | D. | 在0.9mol和1.8mol之间 |
17.下列物质属于分子晶体的化合物是( )
| A. | 石英 | B. | 硫磺 | C. | 干冰 | D. | 食盐 |
4.下列排列顺序不正确的是( )
| A. | 非金属性:F>Cl>S | B. | 熔点:SiO2>KCl>I2 | ||
| C. | 稳定性:HF>H2S>H2O | D. | 碱性:KOH>NaOH>Al(OH)3 |
1.下列各组中的关系正确的是( )
| A. | 同位素:O2和O3 | B. | 同分异构体: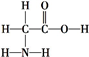 和 和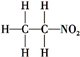 | ||
| C. | 同素异形体:K2O、K2O2、KO2 | D. | 同种物质: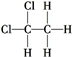 和 和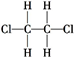 |
2.在一定温度下,恒容的密闭容器中,可逆反应X(g)+3Y(g)?2Z(g)达到平衡(反应最大限度)的标志是( )
| A. | X、Y、Z的浓度不再发生变化 | |
| B. | X、Y、Z三种物质体积分数均相等 | |
| C. | 气体总质量保持不变 | |
| D. | 单位时间消耗3molY,同时生成2molZ |

 .
. ;
;