题目内容
 肼(N2H4)又称联氨,是一种可燃性液体,用作火箭燃料.
肼(N2H4)又称联氨,是一种可燃性液体,用作火箭燃料.(1)肼-空气燃料电池是一种清洁的碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,在负极反应的是
(2)右图是一个电化学装置示意图.用肼--空气燃料电池做此装置的电源.
①如果A为含有锌、银、金、等杂质的粗铜,B为纯铜,C为CuSO4.通电一段时间后,A极质量的减少将
②如果A是铂电极,B是石墨电极,C是氯化钠溶液,则若要制得11.2升Cl2气体(标准状况下),该燃料电池理论上需消耗
分析:(1)燃料电池中,负极上燃料失电子发生氧化反应,正极上氧化剂得电子发生还原反应;
(2))①根据转移电子守恒分析;
②根据电极反应式计算气体的物质的量和肼的质量关系.
(2))①根据转移电子守恒分析;
②根据电极反应式计算气体的物质的量和肼的质量关系.
解答:解:(1)作为燃料电池时,负极发生氧化反应,电解质溶液是20%-30%的KOH溶液,N2H4失去电子被氧化生成N2,电极反应式为N2H4+4OH--4e-=N2+4H2O,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-=4OH-,故答案为:N2H4+4OH--4e-=N2+4H2O;O2+2H2O+4e-=4OH-;
(2)①阳极上金属锌、铜都失电子发生氧化反应,阴极上铜离子得电子发生还原反应而析出铜,根据转移电子守恒知,A电极上质量减少的量大于B极质量增加的量,故答案为:大于;
②生成11.2L氯气转移电子的物质的量=
×2=1mol,根据串联电路中转移电子守恒知,消耗肼的质量=
=0.25 mol,
故答案为:0.25.
(2)①阳极上金属锌、铜都失电子发生氧化反应,阴极上铜离子得电子发生还原反应而析出铜,根据转移电子守恒知,A电极上质量减少的量大于B极质量增加的量,故答案为:大于;
②生成11.2L氯气转移电子的物质的量=
| 11.2L |
| 22.4L/mol |
| 1mol |
| 4 |
故答案为:0.25.
点评:本题考查了原电池和电解池原理,涉及电极反应式的书写、离子放电顺序等知识点,难点是电极反应式的书写,要结合电解质溶液的酸碱性分析.

练习册系列答案
相关题目
 肼(N2H4)又称联氨,是一种可燃性液体,与氧气或氮氧化物反应均可生成氮气和水,用作火箭燃料.
肼(N2H4)又称联氨,是一种可燃性液体,与氧气或氮氧化物反应均可生成氮气和水,用作火箭燃料. 肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用的氧化剂,请回答下列问题:
肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用的氧化剂,请回答下列问题:
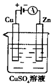 肼(N2H4)又称联氨,可用作火箭燃料.肼一空气燃料电池中的电解质溶液是20%~30%的KOH溶液.该燃料电池可作为如图装置中的电源.下列判断错误的是( )
肼(N2H4)又称联氨,可用作火箭燃料.肼一空气燃料电池中的电解质溶液是20%~30%的KOH溶液.该燃料电池可作为如图装置中的电源.下列判断错误的是( )