��Ŀ����
����Ŀ�������ʯ(��Ҫ�ɷ���Mg9FeSi5O20)��Ϊԭ�������轺����ʽ̼��þ[Mg2(OH)2CO3]�IJ��ֹ�����������ͼ��ʾ��
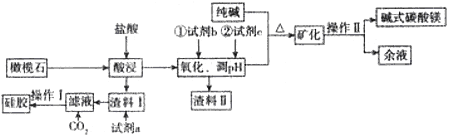
��1��Mg9FeSi5O20����Ԫ�صĻ��ϼ�Ϊ ��Ϊ���þ�Ľ����ʣ��ɲ��õ�������Ҫ��ʩ�� ����II�ijɷ��� ��
��2�����Լ�b���ȼҵ�е�ij��������д������b��Ӧ�����ӷ���ʽ ���Լ�c����;�ǵ�����Һ��pH���Ƚ�ǡ���������� (д��ѧʽ����ͬ)����Һ�����ʵ���Ҫ�ɷ��� ��
��3������I�������� ��д�����ɼ�ʽ̼��þ(ͬʱ����������)�����ӷ���ʽ ��
���𰸡���1��+2�������ʯ���顢���Ͻ�������(����������)��Fe(OH)3
��2�� 2 Fe2+ + Cl2 = 2 Cl�� + 2 Fe3+��MgO ��MgCO3(����������)��NaCl��
��3�����ˡ�ϴ�Ӻ��ٸ�����ˮ��2Mg2+ + 2CO32�� +H2O = Mg2(OH)2 CO3��+ CO2��
��������
�����������1�����ݻ��ϼ۹��������Mg9FeSi5O20����Ԫ�صĻ��ϼ�Ϊ+2�ۣ�Ҫ���þ�Ľ����ʣ���Ҫʹ���ʯ�����ܵ�����Ӵ�������Ӧ���ʹʿɲ��õĴ�ʩ�н��ϼ�ʯ���鼰���Ͻ��跴Ӧ��ϵ�ȣ�������������ΪFe3+��Ȼ����Fe(OH)3��ʽ�����������ʴ�Ϊ��+2�������ʯ���顢���Ͻ������Fe(OH)3��
��2��������Fe2+����ΪFe3+��Ϊ��������������Ӧʹ��MgO,MgCO3�ȵ�����Һ��pH���Լ��е�Na+�� Cl-��û�вμӷ�Ӧ������Һ�����ʵ���Ҫ�ɷ���NaCl���ʴ�Ϊ��2 Fe2+ + Cl2 = 2 Cl�� + 2 Fe3+��MgO ��MgCO3��NaCl��
��3��ͨ��CO2��õ��������������ˡ�ϴ�Ӻ��ٸ�����ˮ������ʽ̼��þ�����֪����Ӧ����Mg2+��CO32����H2O��H2O�������OH-ת��Ϊ������H+��һ����CO32���������ɶ�����̼���ʴ�Ϊ�����ˡ�ϴ�Ӻ��ٸ�����ˮ��2Mg2+ + 2CO32�� +H2O = Mg2(OH)2 CO3��+ CO2����