题目内容
【题目】根据信息书写指定反应的方程式。
(1)请从下列溶液中选择合适的溶液完成指定转化(试剂可以重复选择)。溶液:NH3·H2O、FeSO4、Fe2(SO4)3、HCl、NaCl
①写出SO2→H2SO4的化学方程式:____;
②写出SO2→SO32-的离子方程式:____。
(2)三聚磷酸铝(AlH2P3O10·2H2O)是新一代无公害白色防锈颜料,可由膨润土(主要成分:Al2O3·4SiO2·3H2O;含杂质:FeO、Fe2O3、Na2O等)为原料经过如下流程制备。
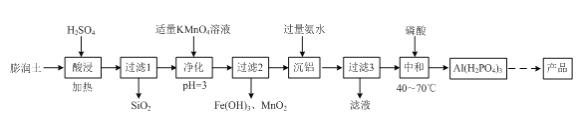
①“酸浸”时Al2O3·4SiO2·3H2O与硫酸反应的化学方程式为____。
②“净化”时发生反应的离子方程式为____。
③“沉铝”时发生反应的离子方程式为____。
【答案】SO2+Fe2(SO4)3+2H2O=== 2FeSO4+2H2SO4 SO2+2NH3·H2O=== SO32-+2NH4++H2O Al2O3·4SiO2·3H2O+3H2SO4![]() Al2(SO4)3+4SiO2+6H2O 3Fe2++MnO4-+7H2O===3Fe(OH)3↓+MnO2↓+5H+ Al3++3NH3·H2O===Al(OH)3↓+3NH4+
Al2(SO4)3+4SiO2+6H2O 3Fe2++MnO4-+7H2O===3Fe(OH)3↓+MnO2↓+5H+ Al3++3NH3·H2O===Al(OH)3↓+3NH4+
【解析】
(1)①SO2→H2SO4,S元素化合价升高,被氧化,作还原剂,需加入氧化剂氧化SO2,以上溶液中Fe2(SO4)3可作氧化剂氧化SO2;
②SO2→SO![]() ,SO2与碱反应可生成SO
,SO2与碱反应可生成SO![]() ,以上溶液中NH3·H2O为碱;
,以上溶液中NH3·H2O为碱;
(2)膨润土(主要成分:Al2O34SiO23H2O;含少量杂质:FeO、Fe2O3、Na2O等)为原料制备三聚磷酸铝[AlH2P3O102H2O],加稀硫酸,Al2O3、FeO、Fe2O3、Na2O转化为离子,SiO2不溶于硫酸,过滤,滤液中含有Al3+、Fe2+、Fe3+,加高锰酸钾溶液,Fe2+被氧化为Fe3+,同时生成的锰离子可再被高锰酸钾氧化成二氧化锰,调节pH值,得氢氧化铁沉淀和二氧化锰沉淀,滤液中主要含有硫酸铝及少量硫酸钠杂质,再加入氨水,得氢氧化铝沉淀,过滤,滤液3中含有硫酸钠和硫酸铵还有氨水,氢氧化铝中加入磷酸,缩合可得三聚磷酸铝,据此解答。
(1)①SO2→H2SO4,S元素化合价升高,被氧化,作还原剂,需加入氧化剂氧化SO2,以上溶液中Fe2(SO4)3可作氧化剂氧化SO2,发生反应的化学方程式为:SO2+Fe2(SO4)3+2H2O=== 2FeSO4+2H2SO4;
故答案为:SO2+Fe2(SO4)3+2H2O=== 2FeSO4+2H2SO4;
②SO2→SO32-,SO2与碱反应可生成SO32-,以上溶液中NH3·H2O为碱,发生反应的离子方程式为:SO2+2NH3·H2O=== SO32-+2NH4++H2O;
故答案为:SO2+2NH3·H2O=== SO32-+2NH4++H2O;
(2)膨润土(主要成分:Al2O34SiO23H2O;含少量杂质:FeO、Fe2O3、Na2O等)为原料制备三聚磷酸铝[AlH2P3O102H2O],加稀硫酸,Al2O3、FeO、Fe2O3、Na2O转化为离子,SiO2不溶于硫酸,过滤,滤液中含有Al3+、Fe2+、Fe3+、Na+,加高锰酸钾溶液,Fe2+被氧化为Fe3+,同时生成的锰离子可再被高锰酸钾氧化成二氧化锰,调节pH值,得氢氧化铁沉淀和二氧化锰沉淀,滤液中主要含有硫酸铝及少量硫酸钠杂质,再加入氨水,得氢氧化铝沉淀,过滤,滤液3中含有硫酸钠和硫酸铵还有氨水,氢氧化铝中加入磷酸,缩合可得三聚磷酸铝,
①加入稀硫酸“酸浸”时,Al2O3、FeO、Fe2O3、Na2O转化为离子,SiO2不溶于硫酸,则Al2O3·4SiO2·3H2O与硫酸反应的化学方程式为Al2O3·4SiO2·3H2O+3H2SO4![]() Al2(SO4)3+4SiO2+6H2O;
Al2(SO4)3+4SiO2+6H2O;
故答案为:Al2O3·4SiO2·3H2O+3H2SO4![]() Al2(SO4)3+4SiO2+6H2O;
Al2(SO4)3+4SiO2+6H2O;
②“净化”时加入高锰酸钾溶液,Fe2+被氧化为Fe3+,同时生成的锰离子可再被高锰酸钾氧化成二氧化锰,调节pH值,得氢氧化铁沉淀和二氧化锰沉淀,发生反应的离子方程式为3Fe2++MnO4-+7H2O===3Fe(OH)3↓+MnO2↓+5H+;
故答案为:3Fe2++MnO4-+7H2O===3Fe(OH)3↓+MnO2↓+5H+;
③滤液中铝元素是以铝离子的形式存在的,加入过量氨水,反应生成氢氧化铝,发生反应的离子方程式为Al3++3NH3·H2O===Al(OH)3↓+3NH4+;
故答案为:Al3++3NH3·H2O===Al(OH)3↓+3NH4+。