题目内容
【题目】我国科学家设计二氧化碳熔盐捕获及电化学转化装置,其示意图如下:
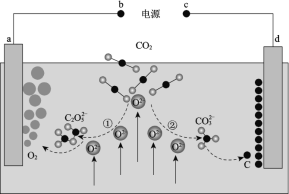
下列说法不正确的是
A.c为电源的负极
B.①②中,捕获CO2时碳元素的化合价均未发生变化
C.d极的电极反应式为![]() + 4e = C + 3O2
+ 4e = C + 3O2
D.转移1mol电子可捕获CO2 2.8 L(标况下)
【答案】D
【解析】
过程①为2CO2+O2-=![]() ,a极电极反应为2
,a极电极反应为2![]() -4e-=O2↑+4CO2,a电极失电子,为阳极,则b电极为电源的正极;过程②为CO2+O2-=
-4e-=O2↑+4CO2,a电极失电子,为阳极,则b电极为电源的正极;过程②为CO2+O2-=![]() ,d极电极反应为
,d极电极反应为![]() +4e-=C+3O2-,d电极得电子,为阴极,则c电极为电源的负极。
+4e-=C+3O2-,d电极得电子,为阴极,则c电极为电源的负极。
A.由以上分析可知,c为电源的负极,A正确;
B.①②中,捕获CO2时发生的反应分别为2CO2+O2-=![]() 、CO2+O2-=
、CO2+O2-=![]() ,碳元素的化合价均未发生变化,B正确;
,碳元素的化合价均未发生变化,B正确;
C.d极为阴极,![]() 得电子生成C 和O2,电极反应式为
得电子生成C 和O2,电极反应式为![]() + 4e= C + 3O2,C正确;
+ 4e= C + 3O2,C正确;
D.将阴、阳极发生的电极反应加和,便得到总反应式为:CO2![]() C+O2↑,转移4mol电子时,消耗1molCO2,则转移1mol电子可捕获CO2 的体积为
C+O2↑,转移4mol电子时,消耗1molCO2,则转移1mol电子可捕获CO2 的体积为![]() =5.6 L(标况下),D不正确;
=5.6 L(标况下),D不正确;
故选D。

练习册系列答案
相关题目