题目内容
实验室用铜制备CuSO4溶液有多种方案,某实验小组给出了以下三种方案: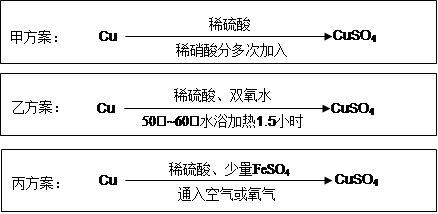
请回答有关问题:
(1)甲方案:
①写出该反应的离子方程式 ;
②为了节约原料,硫酸和硝酸的物质的量之比最佳为,n(H2SO4):n(HNO3)= 。
(2)乙方案:将6.4g铜丝放到90mL 1.5mol·L-1的稀硫酸中,控温在50℃。加入40mL 10%的H2O2,反应0.5小时,升温到60℃,持续反应1小时后,经一系列操作,得CuSO4·5H2O 20.0g【已知有关摩尔质 量:M(Cu)=64g/mol, M(CuSO4·5H2O) =250g/mol】。
①反应时温度控制在50℃~60℃,不宜过高的原因是 ;
②本实验CuSO4·5H2O的产率为 。
(3)丙方案:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,即发生反应,生成硫酸铜。反应完全后,加物质A调节pH至4 ,然后过滤、浓缩、结晶。
①物质A可选用以下的 (填序号);
| A.CaO | B.NaOH | C.CuCO3 | D.Cu2(OH)2CO3 E.Fe2(SO4)3 |
(4)对比甲、乙、丙三种实验方案,丙方案的优点有(写两条):
、 。
(1)①3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O (3分); ②3:2(2分)
(2)①双氧水受热易分解造成损耗(2分); ②80%(3分)
(3)①CD(2分); ②作催化剂(或起催化作用,2分)
(4)无污染;原料利用率高(或常温下反应,耗能少;原料便宜,成本低等)(2分)
解析试题分析:(1)①铜与稀硫酸、稀硝酸的混合液反应生成铜离子、NO、水,离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
②硫酸铜的化学式中Cu2+与SO42-的个数比是1:1,离子方程式中Cu2+与NO3-的个数比是是3:2,所以n(H2SO4):n(HNO3)=3:2;
(2)①因为过氧化氢受热易分解,温度过高,造成过氧化氢的损失,产率降低;
②604gCu的物质的量是0.1mol,硫酸的物质的量是0.135mol,所以硫酸过量,理论上应生成0.1molCuSO4·5H2O,质量是25.0g,实际得到CuSO4·5H2O 20.0g,所以CuSO4·5H2O的产率是20.0g/25.0g×100%=80%;
(3)①加物质A调节pH至4目的是降低溶液酸度,使铁元素沉淀,同时不引入新杂质,所以应选择CuCO3、Cu2(OH)2CO3,二者与硫酸反应生成硫酸铜、二氧化碳气体放出,符合题目要求,而ABE均会引入新杂质,答案选CD。
②反应中加入少量FeSO4可加速铜的氧化,而FeSO4不与溶液中的任何物质反应,所以FeSO4的作用只能是催化剂的作用;
(4)与甲、乙比,丙的优点是不会产生污染,耗能少,原料便宜,节约原料等。
考点:考查硫酸铜的制备实验,对实验的分析能力,优缺点的比较,产率的计算

稀硫酸中插一块铜片,加入下列物质后,可使铜片发生反应的是 ( )
| A.稀盐酸 | B.硫酸钠晶体 | C.硝酸钾晶体 | D.氯化钠晶体 |
某校化学研究性学习小组,在学习金属的冶炼以后对一氧化碳还原金属氧化物的实验非常感兴趣,他们查阅有关资料后发现,一氧化碳的制备可利用甲酸和浓硫酸共热到60~80 ℃发生脱水反应制取:
HCOOH CO↑+H2O
CO↑+H2O
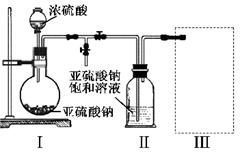
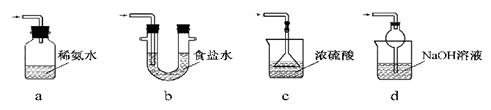
请根据以下各图帮他们组装成一套相对合理的实验装置图(某些装置可重复使用)。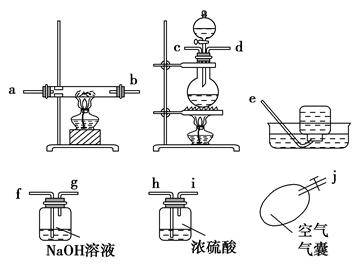
回答以下问题:
(1)合理实验装置的连接顺序是(写小写字母) 。
(2)在反应时一定要先通一会一氧化碳气体,然后再点燃加热氧化铁的酒精灯,原因是 。
| A.因为一般反应从左到右进行 |
| B.排除体系内的空气,使反应过程更安全 |
| C.甲酸与浓硫酸反应可以产生大量的CO |
| D.此反应加热时间长有利于产生CO |
(4)在观察到硬质玻璃管中的物质由 色完全变为 色时停止加热,然后继续 ,原因是防止铁被氧化。
(5)硬质玻璃管中发生反应的化学方程式为 。
(6)该实验的一个优点是把实验过程中的尾气利用排水法收集起来,收集的气体前后有几瓶,分别按收集的先后顺序编号,点燃各个瓶中的气体,中间编号的集气瓶中气体 ,编号最先和最后的集气瓶中气体 ,原因是 。

 H++Cl-+ HClO,其平衡常数表达式为K= 。
H++Cl-+ HClO,其平衡常数表达式为K= 。

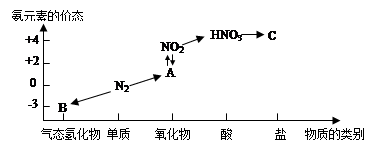
 C
C