题目内容
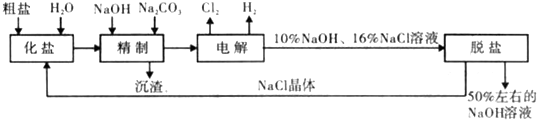
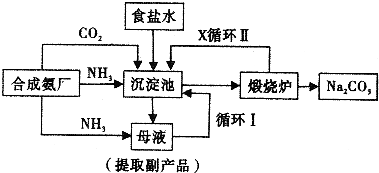
【化学选修2-化学与技术】工业生产纯碱的工艺流程示意图如下:

完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(A来源于石灰窑厂),则B的化学式为
(2)②过滤后滤液中要通入C和D气体,则先通入的C气体是
(3)通入C和D气体后发生反应的化学方程式是
(4)④过滤后,向滤液中通入氨气,加入细小食盐颗粒,析出副产品
(5)写出⑤煅烧发生反应的化学方程式:
分析:(1)粗盐水加入沉淀剂A、B除去粗盐中的杂质镁离子等,沉淀剂A来源于石灰窑厂,所以A、B的化学式为Ca(OH)2、Na2CO3;
(2)工业制纯碱时需先通入氨气,因为氨气的溶解度比二氧化碳大得多,且溶液呈碱性,有利于二氧化碳的吸收;
(3)根据氨气和二氧化碳在水中的溶解性分析对产物的影响,先后通入C和D气体后,滤渣是碳酸氢钠,它的溶解度比碳酸钠小;
(4)滤液主要含有碳酸氢钠和氯化铵等,加入食盐、通入氨气,则铵根离子和氯离子浓度增大,则使氯化铵浓度达到溶解度而析出;
(5)根据碳酸氢钠受热易分解和碳酸钠受热稳定的性质来回答,碳酸氢钠受热分解能生成碳酸钠、水和二氧化碳,加热前后的固体质量差为二氧化碳和水的质量之和,根据差量法计算碳酸氢钠的质量分数.
(2)工业制纯碱时需先通入氨气,因为氨气的溶解度比二氧化碳大得多,且溶液呈碱性,有利于二氧化碳的吸收;
(3)根据氨气和二氧化碳在水中的溶解性分析对产物的影响,先后通入C和D气体后,滤渣是碳酸氢钠,它的溶解度比碳酸钠小;
(4)滤液主要含有碳酸氢钠和氯化铵等,加入食盐、通入氨气,则铵根离子和氯离子浓度增大,则使氯化铵浓度达到溶解度而析出;
(5)根据碳酸氢钠受热易分解和碳酸钠受热稳定的性质来回答,碳酸氢钠受热分解能生成碳酸钠、水和二氧化碳,加热前后的固体质量差为二氧化碳和水的质量之和,根据差量法计算碳酸氢钠的质量分数.
解答:解:(1)粗盐中含有硫酸根离子、碳酸根离子、镁离子,常用的提纯食盐的沉淀剂为氢氧化钙溶液和碳酸钠溶液,沉淀剂A来源于石灰窑厂,所以A是氢氧化钙,B是碳酸钠,故答案为:Na2CO3;
(2)二氧化碳微溶于水,先通入二氧化碳,溶液中生成极少量的碳酸,再通入氨气,生成的产物量少,且易生成碳酸铵,氨气在水中溶解度很大,先通入氨气,溶液中生成较多的一水合氨,再通入CO2,生成的产物量多,且易生成碳酸氢铵,
故答案为:NH3;因为二氧化碳在水中的溶解度小而氨气在水中的溶解度比较大,且通入氨气溶液呈碱性有利于反应进行;
(3)碳酸氢钠的溶解度比碳酸钠小,滤渣是碳酸氢钠,所以先后通入C和D气体后,发生反应NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl,
故答案为:NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl;
(4)先后通入C和D气体后,④过滤后,滤渣是碳酸氢钠,向滤液中通入氨气,加入细小食盐颗粒,溶液中的氯离子和铵根离子的浓度增大,使氯化铵大量析出,故析出的副产品为:NH4Cl,
故答案为:NH4Cl;增大溶液中的氯离子和铵根离子的浓度,使氯化铵大量析出;
(5)煅烧时,碳酸氢钠分解2NaHCO3
Na2CO3+H2O+CO2↑,生成碳酸钠,根据差量法加热前后的固体质量差为二氧化碳和水的质量之和,加热前纯碱的质量为m(加热前),加热后的质量为m(加热后),则加热损失的质量为:m(加热前)-m(加热后),根据2NaHCO3
Na2CO3+H2O+CO2↑,每当有168克碳酸氢钠分解,固体质量减少62克,则纯碱中碳酸氢钠的质量为:
;故纯碱中含有的碳酸氢钠的质量分数为
,
故答案为:
.
(2)二氧化碳微溶于水,先通入二氧化碳,溶液中生成极少量的碳酸,再通入氨气,生成的产物量少,且易生成碳酸铵,氨气在水中溶解度很大,先通入氨气,溶液中生成较多的一水合氨,再通入CO2,生成的产物量多,且易生成碳酸氢铵,
故答案为:NH3;因为二氧化碳在水中的溶解度小而氨气在水中的溶解度比较大,且通入氨气溶液呈碱性有利于反应进行;
(3)碳酸氢钠的溶解度比碳酸钠小,滤渣是碳酸氢钠,所以先后通入C和D气体后,发生反应NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl,
故答案为:NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl;
(4)先后通入C和D气体后,④过滤后,滤渣是碳酸氢钠,向滤液中通入氨气,加入细小食盐颗粒,溶液中的氯离子和铵根离子的浓度增大,使氯化铵大量析出,故析出的副产品为:NH4Cl,
故答案为:NH4Cl;增大溶液中的氯离子和铵根离子的浓度,使氯化铵大量析出;
(5)煅烧时,碳酸氢钠分解2NaHCO3
| ||
| ||
| 168×【m(加热前)-m(加热后)】 |
| 62 |
| 84【m(加热前)-m(加热后)】 |
| 31m(加热前) |
故答案为:
| 84【m(加热前)-m(加热后)】 |
| 31m(加热前) |
点评:本题以工业生产纯碱的工艺流程为背景,考查了物质的提纯、化学实验基本操作、实验结果的处理等知识,(5)差量法的运用是解答本题的难点,题目难度中等.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目