题目内容
【化学--选修2化学与技术】侯德榜制碱法,也叫联合制碱法,其生产流程可简要表示如下图:
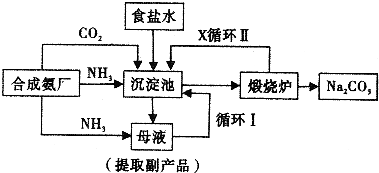
(1)向沉淀池中通入CO2和氨气时,应先通入
(2)沉淀池中发生反应的化学反应方程式是
(3)向母液中通氨气并加入细小食盐颗粒,冷却析出的副产品是
A.增大NH+4的浓度:使NH4Cl更多地析出
B.使NaHCO3更多地析出
C.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
(4)为提高原料氯化钠的利用率,主要是设计了
(5)CO2是制碱工业的重要原料,侯德耪制碱法和氨碱法中CO2的来源有何不同
(6)产品纯碱中含有碳酸氢钠,可以用加热分解的方法测定产品中纯碱的质量分数,已知样品质量为ag,加热至质量不再改变时称重为bg,则纯碱的质量分数为
分析:(1)氨气极易溶于水,二氧化碳在水中的溶解度较小;
(2)饱和食盐水中通入氨气和二氧化碳析出碳酸氢钠晶体;高温下,碳酸氢钠不稳定易分解;
(3)根据反应方程式确定母液中的溶质,根据氨气溶于水后生成氨水,氨水电离成铵根,增大铵根的浓度有利于氯化铵的析出来分析;同时通入氨气使溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度;
(4)循环Ⅰ中的氯化钠有又返回到沉淀池;物质X是二氧化碳;固液分离的方法为过滤;
(5)侯德耪制碱法中CO2的来源于合成氨工业的废气,氨碱法中CO2来源于石灰石煅烧;
(6)根据质量守恒定律可知,加热至质量不再改变,反应后生成的二氧化碳和水的质量之和为(a-b)g,据此求出碳酸钠的质量,再用碳酸钠的质量除以样品质量即可;
(2)饱和食盐水中通入氨气和二氧化碳析出碳酸氢钠晶体;高温下,碳酸氢钠不稳定易分解;
(3)根据反应方程式确定母液中的溶质,根据氨气溶于水后生成氨水,氨水电离成铵根,增大铵根的浓度有利于氯化铵的析出来分析;同时通入氨气使溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度;
(4)循环Ⅰ中的氯化钠有又返回到沉淀池;物质X是二氧化碳;固液分离的方法为过滤;
(5)侯德耪制碱法中CO2的来源于合成氨工业的废气,氨碱法中CO2来源于石灰石煅烧;
(6)根据质量守恒定律可知,加热至质量不再改变,反应后生成的二氧化碳和水的质量之和为(a-b)g,据此求出碳酸钠的质量,再用碳酸钠的质量除以样品质量即可;
解答:解:(1)二氧化碳在水中的溶解度较小,氨气极易溶于水,所以应该先通氨气有利于吸收二氧化碳,
故答案为:NH3;因为CO2溶解度小,而NH3易溶于水,先通入NH3有利于后面CO2的吸收;
(2)氨气、二氧化碳、水和氯化钠发生反应生成碳酸氢钠和氯化铵,反应方程式为NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓,
煅烧炉中碳酸氢钠不稳定,在加热条件下能分解生成碳酸钠、水和二氧化碳,反应方程式为2NaHCO3
Na2CO3+CO2↑+H2O,
故答案为:NH3+CO2+NaCl+H2O═NaHCO3↓+NH4Cl;2NaHCO3
Na2CO3+CO2↑+H2O;
(3)根据NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓及流程图知,母液中溶质为氯化铵,向母液中通氨气加入细小食盐颗粒,冷却析出副产品,通入的氨气和水反应生成一水合氨,一水合氨电离出铵根离子,铵根离子浓度增大有利于析出氯化铵,所以选项A正确;
通入氨气使溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度所以选项C正确,
故答案为:NH4Cl;AC;
(4)循环Ⅰ是将未反应的氯化钠返回沉淀池中,煅烧碳酸氢钠时生成二氧化碳、二氧化碳能循环利用,所以X是CO2,从固液混合物中分离出固体的方法为过滤,
故答案为:Ⅰ;CO2;过滤;
(5)侯德耪制碱法:以食盐、氨和二氧化碳(其中二氧化碳来自合成氨厂用水煤气制取氢气时的废气)为原料来制取纯碱,氨碱法:以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气为原料来制取纯碱,两者CO2的来源不同,
故答案为:前者CO2是由合成氨厂提供,后者CO2是由碳酸钙分解得到;
(6)设原混合物中碳酸钠的质量为X,
2NaHCO3
Na2CO3+H2O+CO2↑ 固体减少的质量
168 106 18 44 62
(a-x)g (a-b)g
列比例式:
=
解得X=
,所以纯碱的质量分数为:
×100%,
故答案为:
×100%;
故答案为:NH3;因为CO2溶解度小,而NH3易溶于水,先通入NH3有利于后面CO2的吸收;
(2)氨气、二氧化碳、水和氯化钠发生反应生成碳酸氢钠和氯化铵,反应方程式为NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓,
煅烧炉中碳酸氢钠不稳定,在加热条件下能分解生成碳酸钠、水和二氧化碳,反应方程式为2NaHCO3
| ||
故答案为:NH3+CO2+NaCl+H2O═NaHCO3↓+NH4Cl;2NaHCO3
| ||
(3)根据NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓及流程图知,母液中溶质为氯化铵,向母液中通氨气加入细小食盐颗粒,冷却析出副产品,通入的氨气和水反应生成一水合氨,一水合氨电离出铵根离子,铵根离子浓度增大有利于析出氯化铵,所以选项A正确;
通入氨气使溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度所以选项C正确,
故答案为:NH4Cl;AC;
(4)循环Ⅰ是将未反应的氯化钠返回沉淀池中,煅烧碳酸氢钠时生成二氧化碳、二氧化碳能循环利用,所以X是CO2,从固液混合物中分离出固体的方法为过滤,
故答案为:Ⅰ;CO2;过滤;
(5)侯德耪制碱法:以食盐、氨和二氧化碳(其中二氧化碳来自合成氨厂用水煤气制取氢气时的废气)为原料来制取纯碱,氨碱法:以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气为原料来制取纯碱,两者CO2的来源不同,
故答案为:前者CO2是由合成氨厂提供,后者CO2是由碳酸钙分解得到;
(6)设原混合物中碳酸钠的质量为X,
2NaHCO3
| ||
168 106 18 44 62
(a-x)g (a-b)g
列比例式:
| 168 |
| a-x |
| 62 |
| a-b |
| 84b-53a |
| 31 |
| 84b-53a |
| 31a |
故答案为:
| 84b-53a |
| 31a |
点评:本题考查了侯德榜制碱法实验方案的设计,明确碳酸钠、碳酸氢钠、氨气、二氧化碳的性质,掌握工艺流程和反应原理是解题关键,题目难度中等.

练习册系列答案
 同步奥数系列答案
同步奥数系列答案
相关题目