题目内容
【化学-选修2化学与技术】(l)火法炼锌是将闪锌矿(主要成分是ZnS)通过浮选焙烧使它转化为氧化锌,再把氧化锌和焦炭混合,在鼓风炉中加热到1100~1300℃,使锌蒸馏出来.
①写出火法炼锌的主要反应:焙烧反应:
②从保护环境和充分利用原料角度看如何处理和利用产生的烟气?
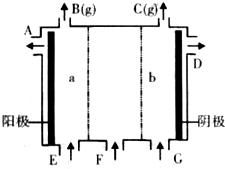
(2)工业上冶炼铝就是电解氧化铝
①冶炼铝的电解槽中的阴极和阳极材料均用石油炼制和煤的干馏产品
②氧化铝的熔点很高,在铝的冶炼中要加入冰晶石(Na3AlF),其作用是
③工业上冶炼铝时用的原料是Al2O3,而不是AlCl3,其原因是
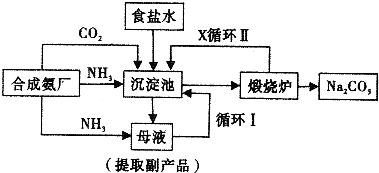
(3)工业上“联合制碱法”中主要反应的化学方程式是
(4)磁酸钙是制玻璃的原料之一,工业上制玻璃是在玻璃熔炉中进行,其中反应之一为:CaCO3+SiO2
| ||
分析:(1)①焙烧中硫化锌与氧气在高温下反应生成氧化锌和二氧化硫;鼓风炉中碳与氧气在高温下反应生成一氧化碳、氧化锌在高温下被一氧化碳还原成金属锌,据此写出反应的化学方程式;
②闪锌矿主要含ZnS,在焙烧时生成二氧化硫气体,可用于生产硫酸;
(2)①冶炼铝的电解槽中的阴极和阳极材料均为惰性电极;
②氧化铝的熔点很高,在铝的冶炼中要加入冰晶石可以降低氧化铝的熔化温度;
③氯化铝为共价化合物,熔化后不导电,而氧化铝为离子化合物;
(3)根据工业上“联合制碱法”的原理写出反应的化学方程式;联合制碱法中CO2来源于合成氨工业的废气;
(4)碳酸钙在高温下能够发生反应:CaCO3
CaO+CO2↑,所以生成二氧化碳的物质的量就等于碳酸钙的物质的量,与反应中二氧化硅的物质的量无关,据此计算出生成标况下二氧化碳的体积.
②闪锌矿主要含ZnS,在焙烧时生成二氧化硫气体,可用于生产硫酸;
(2)①冶炼铝的电解槽中的阴极和阳极材料均为惰性电极;
②氧化铝的熔点很高,在铝的冶炼中要加入冰晶石可以降低氧化铝的熔化温度;
③氯化铝为共价化合物,熔化后不导电,而氧化铝为离子化合物;
(3)根据工业上“联合制碱法”的原理写出反应的化学方程式;联合制碱法中CO2来源于合成氨工业的废气;
(4)碳酸钙在高温下能够发生反应:CaCO3
| ||
解答:解:(1)①由题中信息可知,闪锌矿(主要成分是ZnS)通过浮选焙烧使它转化为氧化锌,反应的化学方程式为:2ZnS+3O2
2ZnO+2SO2;
氧化锌和焦炭混合,在鼓风炉中加热到1100~1300℃,使锌蒸馏出来,反应的化学方程式为:2C+O2
2C0或ZnO+CO
Zn+CO2,
故答案为:2ZnS+3O2
2ZnO+2SO2;2C+O2
2C0或ZnO+CO
Zn+CO2;
②闪锌矿主要含ZnS,在焙烧时生成二氧化硫气体,如随意排放会污染环境,可用于生产硫酸,
故答案为:将烟道气净化,用于生产硫酸;
(2)①电解法冶炼金属铝需要使用惰性电极,石油炼制和煤的干馏产品中石墨(或碳)可以作为惰性电极电解冶炼铝,
故答案为:石墨(或碳);
②由于氧化铝熔点高,为了降低氧化铝熔化温度,节约能源,在铝的冶炼中要加入冰晶石(Na3AlF),
故答案为:降低氧化铝熔化温度,节约能源;
③由于氧化铝为离子化合物,熔化后能够导电,而氯化铝是共价化合物,熔化后不导电,无法电解氯化铝获得金属铝,
故答案为:氧化铝熔化后能够导电,氯化铝是共价化合物,熔化后不导电;
(3)联合制碱法是在氨的饱和NaCl溶液中二氧化碳气体,反应生成碳酸氢钠,解热碳酸氢钠即可制备碳酸钠,反应的有关方程式为,NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl;2NaHCO3
Na2CO3+CO2↑+H2O;CO2是制碱工业的重要原料,联合制碱法中CO2来源于合成氨工业的废气,
故答案为:NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl、2NaHCO3
Na2CO3+CO2↑+H2O;合成氨厂;
(4)1000ag CaCO3的物质的量为:
=10mol,在高温下加热SiO2和CaCO3固体混合物发生反应为:CaCO3
CaO+CO2↑,CaO+SiO2
CaSiO3,反应生成二氧化碳的物质的量等于碳酸钙的物质的量,即10amol二氧化碳,标准状况下二氧化碳的体积为:22.4L/mol×10a=224a,
故答案为:224a.
| ||
氧化锌和焦炭混合,在鼓风炉中加热到1100~1300℃,使锌蒸馏出来,反应的化学方程式为:2C+O2
| ||
| ||
故答案为:2ZnS+3O2
| ||
| ||
| ||
②闪锌矿主要含ZnS,在焙烧时生成二氧化硫气体,如随意排放会污染环境,可用于生产硫酸,
故答案为:将烟道气净化,用于生产硫酸;
(2)①电解法冶炼金属铝需要使用惰性电极,石油炼制和煤的干馏产品中石墨(或碳)可以作为惰性电极电解冶炼铝,
故答案为:石墨(或碳);
②由于氧化铝熔点高,为了降低氧化铝熔化温度,节约能源,在铝的冶炼中要加入冰晶石(Na3AlF),
故答案为:降低氧化铝熔化温度,节约能源;
③由于氧化铝为离子化合物,熔化后能够导电,而氯化铝是共价化合物,熔化后不导电,无法电解氯化铝获得金属铝,
故答案为:氧化铝熔化后能够导电,氯化铝是共价化合物,熔化后不导电;
(3)联合制碱法是在氨的饱和NaCl溶液中二氧化碳气体,反应生成碳酸氢钠,解热碳酸氢钠即可制备碳酸钠,反应的有关方程式为,NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl;2NaHCO3
| ||
故答案为:NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl、2NaHCO3
| ||
(4)1000ag CaCO3的物质的量为:
| 1000ag |
| 100g/mol |
| ||
| ||
故答案为:224a.
点评:本题考查了金属的冶炼原理、电解原理及其应用、联合制碱法原理,题目难度中等,试题涉及了锌、铝的冶炼方法、化学方程式的书写、化学计算等知识,其中(4)为易错点,注意碳酸钙在高温下能够分解生成二氧化碳,与二氧化硅的物质的量无关.

练习册系列答案
相关题目