题目内容
【题目】某工厂排放的废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42-。某研究性小组利用这种废液来制取较纯净的氯化钾晶体及液溴,他们设计了如下的流程(提示:图中试剂a的作用是将Br-转化为Br2)
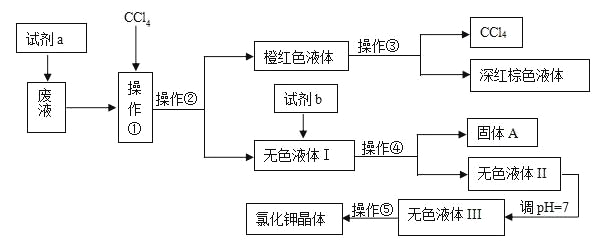
试剂b需要从以下试剂中选择:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、稀盐酸
(1)操作①②③④⑤的名称是________(填序号)。
A. 萃取、过滤、分液、过滤、蒸发结晶
B. 萃取、分液、蒸馏、过滤、蒸发结晶
C. 分液、萃取、过滤、过滤、蒸发结晶
D. 萃取、分液、分液、过滤、蒸发结晶
(2)除去无色液体Ⅰ中的Ca2+、Mg2+、SO42-,选出试剂b(试剂b代表一组试剂)所代表的试剂,按滴加顺序依次是_____________________________________________________________。
(3)调节pH=7的作用是________________________________________,所用的试剂是___________(填名称)
(4)操作⑤中用到的瓷质仪器名称是________________
【答案】BBaCl2溶液、饱和K2CO3溶液、KOH溶液(或KOH溶液、BaCl2溶液、饱和K2CO3溶液或BaCl2溶液、KOH溶液、饱和K2CO3溶液)除去过量的KOH和K2CO3稀盐酸蒸发皿
【解析】
由图示制备流程为:废液中加入双氧水,将溴离子氧化成溴单质,然后加入四氯化碳萃取、分液分离出溴,操作③蒸馏得到四氯化碳和溴单质;无色液体Ⅰ中含有K+、Cl-、Ca2+、Mg2+、SO42-,分别加入BaCl2、K2CO3、KOH溶液过滤后得到无色溶液Ⅱ和固体A,再调节溶液Ⅱ的pH除去碳酸根离子、氢氧根离子,得到无色溶液Ⅲ,最后蒸发结晶获得氯化钾固体。
(1)加入CCl4的目的是萃取;萃取后的操作是将有机层与水层分开,分液;从含有溴的CCl4溶液中分离得到CCl4和液溴的操作,是将两种相互混溶的液体进行蒸馏;操作④完成后得到固体A和无色液体I,分离固体和液体的操作是过滤;操作⑤是从溶液中得到能溶解于水的氯化钾晶体,是蒸发结晶;
(2)除去Ca2+,选用饱和K2CO3溶液;除去Mg2+,选用KOH溶液;除去SO42-,选用BaCl2溶液;
(3)无色液体Ⅱ中还含有杂质离子CO32-和OH-;用pH试纸测定至pH=7;
(4)操作⑤是蒸发结晶,需要使用的仪器为蒸发皿.
制备流程为:废液中加入双氧水,将溴离子氧化成溴单质,加入四氯化碳后萃取、分液分离出溴,通过操作③蒸馏得到四氯化碳和溴单质;无色液体Ⅰ中含有K+、Cl-、Ca2+、Mg2+、SO42-,分别加入BaCl2、K2CO3、KOH溶液过滤后得到无色溶液Ⅱ和固体A,再调节溶液Ⅱ的pH除去碳酸根离子、氢氧根离子,得到无色溶液Ⅲ,通过蒸发结晶获得氯化钾固体。
(1)由流程图知,无色液体Ⅰ中含有K+、Cl-、Ca2+、Mg2+、SO42-,无色液体Ⅲ中只含有K+、Cl-,则试剂b的作用是除去Ca2+、Mg2+、SO42-;操作①是萃取,操作②是分液,将互不相溶的两种液体分开,操作③是蒸馏,将沸点不同、互溶的两液体分开,操作④是过滤将溶液与沉淀分开,操作⑤是结晶,将KCl从其水溶液中提取出来,操作①、②、③、④、⑤的名称是:萃取、分液、蒸馏、过滤、蒸发结晶,则B正确,故选B;
(2)由于除杂时除杂试剂需过量,且不能引入新杂质,所以除去Ca2+,选用饱和K2CO3溶液;除去Mg2+,选用KOH溶液;除去SO42-,选用BaCl2溶液.而且只要满足BaCl2溶液在饱和K2CO3溶液之前加入即可,故滴加顺序依次为:BaCl2溶液、饱和K2CO3溶液、KOH溶液(或KOH溶液、BaCl2溶液、饱和K2CO3溶液或BaCl2溶液、KOH溶液、饱和K2CO3溶液);
(3)由以上知,无色液体Ⅱ中还含有杂质离子CO32-和OH-,需用盐酸来除去过量的OH-及CO32-,调节pH=7的操作方法是滴加盐酸,无气体产生时,用pH试纸测定至pH=7。
(4)由于操作⑤是蒸发结晶,所以该操作用到的瓷质仪器是蒸发皿。

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案【题目】镧系为元素周期表中第ⅢB族、原子序数为57~71的元素。
(1)镝(Dy)的基态原子电子排布式为[Xe]4f106s2,画出镝(Dy)原子外围电子排布图:___________。
(2)高温超导材料镧钡铜氧化物中含有Cu3+,基态时Cu3+ 的电子排布式为________________。
(3)观察下面四种镧系元素的电离能数据,判断最有可能显示+3 价的元素是___________(填元素名称)。几种镧系元素的电离能(单位:kJ mol-1)
元素 | I1 | I2 | I3 | I4 |
Yb(镱) | 604 | 1217 | 4494 | 5014 |
Lu(镥) | 532 | 1390 | 4111 | 4987 |
La(镧) | 538 | 1067 | 1850 | 5419 |
Ce(铈) | 527 | 1047 | 1949 | 3547 |
(4)元素铈(Ce)可以形成配合物(NH4)2[Ce(NO3)6]。
①组成配合物的四种元素,电负性由大到小的顺序为________________(用元素符号表示)。
②写出氮的最简单气态氢化物水溶液中存在的氢键:__________________(任写一种)。
③元素Al 也有类似成键情况,气态氯化铝分子表示为(AlCl3)2,分子中Al 原子杂化方式为_____________,分子中所含化学键类型有______________(填字母)。
a.离子键 b.极性键 C.非极性键 d.配位键
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中镨原子位于面心和顶点,则PrO2(二氧化镨)的晶胞中有________个氧原子;已知晶胞参数为a pm,密度为ρ g· cm-3,NA=_____________ (用含a、ρ的代数式表示)。
【题目】下述实验方案能达到实验目的的是( )
编号 | A | B | C | D |
实验方案 |
|
|
|
|
实验目的 | 实验室制备乙酸乙酯 | 分离乙酸和水 | 验证溴乙烷在氢氧化钠乙醇溶液中发生消去反应产生的乙烯 | 收集乙烯并验证它与溴水发生加成反应 |
A. A B. B C. C D. D






