题目内容
【题目】镧系为元素周期表中第ⅢB族、原子序数为57~71的元素。
(1)镝(Dy)的基态原子电子排布式为[Xe]4f106s2,画出镝(Dy)原子外围电子排布图:___________。
(2)高温超导材料镧钡铜氧化物中含有Cu3+,基态时Cu3+ 的电子排布式为________________。
(3)观察下面四种镧系元素的电离能数据,判断最有可能显示+3 价的元素是___________(填元素名称)。几种镧系元素的电离能(单位:kJ mol-1)
元素 | I1 | I2 | I3 | I4 |
Yb(镱) | 604 | 1217 | 4494 | 5014 |
Lu(镥) | 532 | 1390 | 4111 | 4987 |
La(镧) | 538 | 1067 | 1850 | 5419 |
Ce(铈) | 527 | 1047 | 1949 | 3547 |
(4)元素铈(Ce)可以形成配合物(NH4)2[Ce(NO3)6]。
①组成配合物的四种元素,电负性由大到小的顺序为________________(用元素符号表示)。
②写出氮的最简单气态氢化物水溶液中存在的氢键:__________________(任写一种)。
③元素Al 也有类似成键情况,气态氯化铝分子表示为(AlCl3)2,分子中Al 原子杂化方式为_____________,分子中所含化学键类型有______________(填字母)。
a.离子键 b.极性键 C.非极性键 d.配位键
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中镨原子位于面心和顶点,则PrO2(二氧化镨)的晶胞中有________个氧原子;已知晶胞参数为a pm,密度为ρ g· cm-3,NA=_____________ (用含a、ρ的代数式表示)。
【答案】 ![]() [Ar]3d8(或1s22s22p63s23p63d8) 镧 O>N>H>Ce N-H…(或 N-H…N或O-H…N或O-H…O) sp3 bd 8
[Ar]3d8(或1s22s22p63s23p63d8) 镧 O>N>H>Ce N-H…(或 N-H…N或O-H…N或O-H…O) sp3 bd 8 ![]()
【解析】(1).根据镝(Dy)的基态原子电子排布式[Xe]4f106s2可知,镝(Dy)原子外围4f能级上有10个电子,6s能级上有2个电子,则其外围电子排布图为:![]() ,故答案为:
,故答案为:![]() ;
;
(2).Cu是 29号元素,基态原子的电子排布式为:[Ar]3d104s1,高温超导材料镧钡铜氧化物中含有Cu3+,说明Cu失去3个电子,则基态时Cu3+的电子排布式为:[Ar]3d8 (或1s22s22p63s23p63d8),故答案为:[Ar]3d8 (或1s22s22p63s23p63d8);
(3).第三电离能与第一电离能、第二电离能相差越小,第三个电子越容易失去,+3价可能性越大,在上述表中,镧的I1、I2和I3最接近,则最有可能显示+3 价的元素是镧,故答案为:镧;
(4). ①.元素铈(Ce)可以形成配合物(NH4)2[Ce(NO3)6],组成配合物的四种元素中,因元素非金属性越强,电负性越大,则O>N>H,又因Ce是金属,其电负性在四种元素中最小,所以电负性大小顺序为:O>N>H>Ce,故答案为:O>N>H>Ce;
② . N和 O元素的电负性强,则NH3的水溶液中存在的氢键有:N-H…O(或 N-H…N或O-H…N或O-H…O),故答案为:N-H…O(或 N-H…N或O-H…N或O-H…O);
③ .在气态氯化铝 (AlCl3)2中,每个Al原子与4个Cl原子形成4个σ键,则Al原子的杂化方式为sp3,在该分子中,与Al原子形成极性共价键的两个Cl原子中,有一个是配位键,氯原子提供电子,铝原子提供空轨道,故答案为:sp3;bd;
(5).PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中镨原子位于面心和顶点,所以晶胞中镨原子的个数为:6×1/2+8×1/8=4,则氧原子个数为:4×2=8;根据上述分析可知,一个二氧化镨晶胞中含有4个PrO2,则ρ=![]() =
=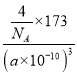 ,则NA=
,则NA= (或
(或![]() ),故答案为:8;
),故答案为:8;  (或
(或![]() );
);

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
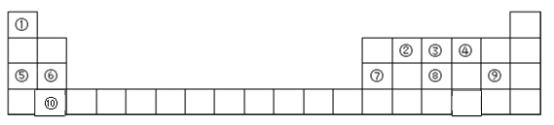
名师点睛字词句段篇系列答案【题目】下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1) 在这些元素中,化学性质最不活泼的是:_________(填具体元素符号,下同),②③⑤元素的原子半径由大到小的顺序为______________________ 。
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是____________/span>,碱性最强的化合物的电子式是:______________________________。
(3) 最高价氧化物是两性氧化物的元素是____;写出该氧化物与氢氧化钠反应的离子方程式_____。
(4) 用电子式表示元素④与⑥的化合物的形成过程:______________,该化合物属于__________(填 “共价”或“离子”)化合物。
(5)写出①与③形成的化合物的电子式____、结构式为___,该化合物的晶体属于_____。
【题目】Ⅰ.水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的某种方法过程如图所示:

(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是_____________,还可使用__________代替硝酸。
(2)沉淀A的主要成分是________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为____________。
(3)加氨水过程中加热的目的是_____。沉淀B的主要成分为_______、_________(填化学式)。
Ⅱ、已知25℃时草酸的电离常数为K1=5.0×10-2,K2=5.4×10-5.草酸钙的Kap=4.0×10-8.碳酸钙的Ksp=2.5×10-9.不同温度下水的离子积常数见下表:
t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
Kw/10-14 | 0.134 | 0.292 | 0.681 | 1.00 | 2.92 | 5.57 | 38.0 | 55.0 |
(1)计算25℃时KHC2O4溶液的水解平衡常数Kb=_____;写出水溶液中草酸的电离方程式_____;常温下将0.2mol/L的KOH溶液10mL与0.2mol/L的草酸溶液20mL混合后溶液显________性。(填“酸性”“中性”或“无法确定”)
(2)25℃时向20mL草酸钙的饱和溶液中逐滴加入8.0×10-4mol/L的碳酸钾溶液10mL,能否产生沉淀,_______(填“能”或“否”). 碳酸钙转化为草酸钙的离子方程式为______,列式计算该反的平衡常数K=_________。
(3)90℃时,将0.005mol/L的氢氧化钙溶液20mL与0.0012mol/L的草酸溶液20mL混合,则混合后溶液的pH______。(可能用到的对数:lg38=1.6,lg26=2.4,lg2=0.3)