题目内容
在25 ℃时,用石墨电极电解2.0 L 2.5 mol·L-1CuSO4溶液,如有0.20 mol电子发生转移,请回答下列问题:
(1)阴极发生 反应,
电极反应式为 ;
(2)阳极发生 反应,
电极反应式为 ;
(3)电解后得到的铜的质量是 ,得到氧气的体积是 (标准状况),溶液的pH是 ;
(4)如果用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差 ,电解液的pH 。
(1)阴极发生 反应,
电极反应式为 ;
(2)阳极发生 反应,
电极反应式为 ;
(3)电解后得到的铜的质量是 ,得到氧气的体积是 (标准状况),溶液的pH是 ;
(4)如果用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差 ,电解液的pH 。
(1)还原 2Cu2++4e-=2Cu
(2)氧化 4OH--4e-=2H2O+O2↑
(3)6.4 g 1.12 L 1
(4)12.8 g 不变
(2)氧化 4OH--4e-=2H2O+O2↑
(3)6.4 g 1.12 L 1
(4)12.8 g 不变
用石墨电极电解CuSO4溶液:
阳极反应式:4OH--4e-=2H2O+O2↑,
阴极反应式:2Cu2++4e-=2Cu。
当线路中有0.20 mol电子转移时,析出铜的质量为
m(Cu)=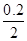 mol×64 g·mol-1=6.4 g。
mol×64 g·mol-1=6.4 g。
产生O2的体积
V(O2)=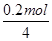 ×22.4 L·mol-1=1.12 L。
×22.4 L·mol-1=1.12 L。
c(H+)=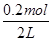 =0.1 mol/L,pH=-lg 0.1=1。
=0.1 mol/L,pH=-lg 0.1=1。
若用Cu片代替石墨电极,则该装置为电镀池,电解后溶液pH不变。当转移0.2 mol电子时,阳极溶解6.4 g,Cu阴极析出6.4 g Cu,则两极质量差为6.4+6.4=12.8(g)。
阳极反应式:4OH--4e-=2H2O+O2↑,
阴极反应式:2Cu2++4e-=2Cu。
当线路中有0.20 mol电子转移时,析出铜的质量为
m(Cu)=
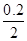 mol×64 g·mol-1=6.4 g。
mol×64 g·mol-1=6.4 g。产生O2的体积
V(O2)=
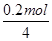 ×22.4 L·mol-1=1.12 L。
×22.4 L·mol-1=1.12 L。c(H+)=
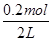 =0.1 mol/L,pH=-lg 0.1=1。
=0.1 mol/L,pH=-lg 0.1=1。若用Cu片代替石墨电极,则该装置为电镀池,电解后溶液pH不变。当转移0.2 mol电子时,阳极溶解6.4 g,Cu阴极析出6.4 g Cu,则两极质量差为6.4+6.4=12.8(g)。

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目