题目内容
氯碱工业中电解饱和食盐水的原理示意图如下图所示:
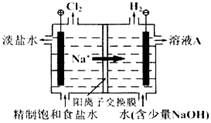
(1)溶液A的溶质是 ;
(2)电解饱和食盐水的离子方程式是 ;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用 ;
(4)电解所用的盐水需精制。去除有影响的Ca2+、Mg2+、NH4+、SO42-[c(SO42->c(Ca2+)]。精致流程如下(淡盐水和溶液A来自电解池):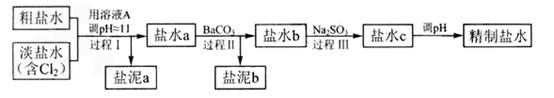
①盐泥a除泥沙外,还含有的物质是 。
②过程Ⅰ中将NH4+转化为N2的离子方程式是 。 ③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有 。

(1)溶液A的溶质是 ;
(2)电解饱和食盐水的离子方程式是 ;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用 ;
(4)电解所用的盐水需精制。去除有影响的Ca2+、Mg2+、NH4+、SO42-[c(SO42->c(Ca2+)]。精致流程如下(淡盐水和溶液A来自电解池):

①盐泥a除泥沙外,还含有的物质是 。
②过程Ⅰ中将NH4+转化为N2的离子方程式是 。 ③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有 。
(1)NaOH
(2)2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
(3)氯气和水反应,Cl2+H2O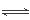 HCl+HClO,增大HCl的浓度可使平衡向逆向移动,减少氯气在水中的溶解度,有利于氯气的溢出。
HCl+HClO,增大HCl的浓度可使平衡向逆向移动,减少氯气在水中的溶解度,有利于氯气的溢出。
(4)①Mg(OH)2 ②2NH4++3Cl2+8OH-=8H2O+6Cl-+N2↑ ③SO42- Ca2+
(2)2Cl-+2H2O
 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑(3)氯气和水反应,Cl2+H2O
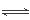 HCl+HClO,增大HCl的浓度可使平衡向逆向移动,减少氯气在水中的溶解度,有利于氯气的溢出。
HCl+HClO,增大HCl的浓度可使平衡向逆向移动,减少氯气在水中的溶解度,有利于氯气的溢出。(4)①Mg(OH)2 ②2NH4++3Cl2+8OH-=8H2O+6Cl-+N2↑ ③SO42- Ca2+
(1)电解时,阴极H+放电,阳极Cl-放电,因此溶液中溶质是NaOH。
(2)电解饱和食盐水的离子方程式为2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
(3)因为阳极上产生Cl2,而氯气能溶解于水,产能发生Cl2+H2O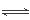 HCl+HClO,根据平衡移动原理知,增大盐酸的浓度可使平衡向逆向移动,这样减少了氯气的溶解度,有利于氯气的溢出。
HCl+HClO,根据平衡移动原理知,增大盐酸的浓度可使平衡向逆向移动,这样减少了氯气的溶解度,有利于氯气的溢出。
(4)由于溶解中含有Mg2+,所以用NaOH调节溶液的pH时,会产生Mg(OH)2沉淀,即盐泥a中还含有Mg(OH)2。淡盐水中含有氯气,氯气具有强氧化性,
可将NH4+氧化为N2,而氯气被还原成Cl-,方程式为2NH4++3Cl2+8OH-=8H2O+6Cl-+N2↑;沉淀转化的实质是沉淀溶解平衡的移动,一般说来,溶解度相对大的容易转化为溶解度更小的沉淀,加入BaCO3后,溶液中的SO42-更容易生成更难溶的BaSO4沉淀,由于Ca2+的存在,还会生成CaCO3沉淀。
(2)电解饱和食盐水的离子方程式为2Cl-+2H2O
 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑(3)因为阳极上产生Cl2,而氯气能溶解于水,产能发生Cl2+H2O
 HCl+HClO,根据平衡移动原理知,增大盐酸的浓度可使平衡向逆向移动,这样减少了氯气的溶解度,有利于氯气的溢出。
HCl+HClO,根据平衡移动原理知,增大盐酸的浓度可使平衡向逆向移动,这样减少了氯气的溶解度,有利于氯气的溢出。(4)由于溶解中含有Mg2+,所以用NaOH调节溶液的pH时,会产生Mg(OH)2沉淀,即盐泥a中还含有Mg(OH)2。淡盐水中含有氯气,氯气具有强氧化性,
可将NH4+氧化为N2,而氯气被还原成Cl-,方程式为2NH4++3Cl2+8OH-=8H2O+6Cl-+N2↑;沉淀转化的实质是沉淀溶解平衡的移动,一般说来,溶解度相对大的容易转化为溶解度更小的沉淀,加入BaCO3后,溶液中的SO42-更容易生成更难溶的BaSO4沉淀,由于Ca2+的存在,还会生成CaCO3沉淀。

练习册系列答案
相关题目


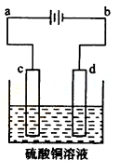
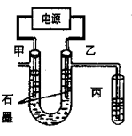
 CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题: