题目内容
【题目】某储氢的碳纳米管二次电池的工作原理如图,该电池的电解质为6 mol·L-1的KOH溶液。下列说法正确的是
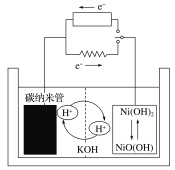
A.放电过程中,碳纳米管的质量一直保持恒重
B.放电时正极附近溶液的pH减小
C.充电时阳极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-
D.该二次电池的工作原理为H2+2NiO(OH)![]() 2Ni(OH)2
2Ni(OH)2
【答案】D
【解析】
放电时相当于是原电池,充电时相当于是电解池,结合原电池、电解池的工作原理和装置图分析解答。
A、放电过程相当于是原电池,利用图示可知放电时储有氢气的碳纳米管中H2失电子发生氧化反应:H2-2e-+2OH-=2H2O,放电过程中,碳纳米管的质量不断减少,A项错误;
B、放电时正极上NiO(OH)得电子发生还原反应:NiO(OH)+e-+H2O=Ni(OH)2+OH-,因此放电时正极附近溶液的pH增大,B项错误;
C、充电时相当于是电解池,阳极应发生氧化反应,充电时阳极反应为Ni(OH)2+OH--e-=NiO(OH)+H2O,C项错误;
D、将正、负极的电极反应式相加可知电池工作原理为H2+2NiO(OH)![]() 2Ni(OH)2,D项正确。
2Ni(OH)2,D项正确。
答案选D。

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目