题目内容
【题目】一定条件下,可逆反应C(s)+CO2(g)![]() 2CO(g),达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积:④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是( )
2CO(g),达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积:④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是( )
A.①②③④B.①③
C.④②D.①③④
【答案】B
【解析】
①升高温度,化学反应的正反应、逆反应的速率都加快,①符合;
②由于碳单质是固体,所以增加反应物C的用量,化学反应速率不变,②不符合;
③缩小反应体系的体积,反应物、生成物的浓度都增大,正反应、逆反应的速率都加快,③符合;
④减小体系中CO的量,即减小生成物的浓度,在这一瞬间,由于反应物的浓度不变,正反应速率不变,生成物的浓度减小,v正>v逆,化学平衡正向移动。随着反应的进行,反应物的浓度逐渐减小,正反应速率逐渐减小,最终正反应、逆反应速率相等,达到新的平衡状态,④不符合;
故上述措施中一定能使反应的正反应速率显著加快的是①③;
答案选B。

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
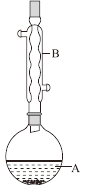
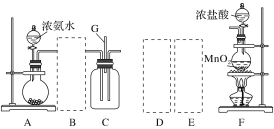
直通贵州名校周测月考直通名校系列答案【题目】某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中A、F为氨气和氯气的发生装置,C为纯净、干燥的氯气与氨气反应的装置。
备选装置 | ||
|
|
|
Ⅰ | Ⅱ | Ⅲ |
请回答下列问题:
(1)装置F中发生反应的离子方程式是___________________________________。
(2)装置A中的烧瓶内固体可选用________(填字母)。
A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从如图的备选装置中选择,并将编号填入下列空格:
B:________、D:________、E:________。
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为:____________________________________;
(5)装置C内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案确定该白色固体中的阳离子:_______________________________________