题目内容
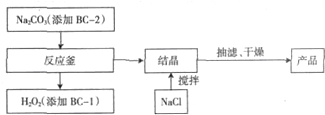
17. 硫代硫酸钠(Na2S2O3•5H2O)是一种脱氯剂,它易溶于水,难溶于乙醇,40~45℃熔化,48℃分解,由硫化钠和亚硫酸钠制备,涉及的反应原理为:
硫代硫酸钠(Na2S2O3•5H2O)是一种脱氯剂,它易溶于水,难溶于乙醇,40~45℃熔化,48℃分解,由硫化钠和亚硫酸钠制备,涉及的反应原理为:2Na2S+3SO2═2Na2SO3+3S↓
SO2+Na2CO3═Na2SO3+CO2
Na2SO3+S═Na2S2O3
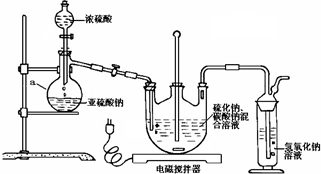
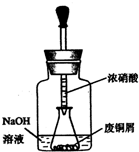
S2O32-+2H+═S↓+SO2↑+H2O.其反应装置如图.
实验操作步聚为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节螺旋夹,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电磁搅拌器搅动.
②至析出的硫不再消失,控制溶液的pH,停止通入SO2气体.
③抽滤所得的滤液,转移至蒸发皿中,水浴加热浓缩,直到溶液表面出现晶膜.
④冷却结晶、过滤、洗涤.
⑤将晶体放入烘箱中,在40~450C左右干燥50~60min,称量.
请回答以下问题:
(1)仪器a的名称是蒸馏烧瓶;
(2)步骤②中,溶液的pH应控制的范围是D.
A.pH=1 B.pH<7 C.pH=7 D. pH>7
(3)装置图中氢氧化钠的作用是吸收未反应的SO2、H2S等酸性气体.
(4)步骤③中不能将溶液蒸发至干的原因是蒸发至干,会使硫代硫酸钠失去结晶水并发生分解;晶膜通常在溶液表面出现的原因是因为溶液表面温度较低.
(5)步骤④中洗涤硫代硫酸钠晶体试剂的结构式是
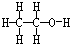 .
.(6)下列有关抽滤的说法中,正确的是A、B、D.
A.为了检验洗涤是否完全,应拔下吸滤瓶与安全瓶之间橡皮管,从吸滤瓶上口倒出少量滤液于试管中进行相关实验
B.抽滤前先用溶剂将滤纸湿润,使滤纸与漏斗底部贴紧
C.抽滤结束时应先关抽气泵,后抽掉抽滤瓶接管
D.在洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物
(7)称取一定质量的产品配置成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中用基准物质K2Cr2O7加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+═3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-═2I-+S4O62-,滴定终点的现象为溶液由蓝色恰好变成无色,且半分钟不恢复,间接碘量法滴定过程中造成实验结果偏低的是A.
A.滴定管未用Na2S2O3溶液润洗 B.滴定终点时俯视读数
C.锥形瓶用蒸馏水润洗 D.滴定管尖嘴处滴定前有气泡滴定后气泡消失.
分析 (1)根据装置图分析;
(2)Na2S2O3在酸性条件下会反应生成S和二氧化硫;
(3)二氧化硫是污染性气体不能排放空气中,需要用氢氧化钠溶液吸收;
(4)由题给信息:硫代硫酸钠“加热易分解”回答即可;溶液表面的温度较低,据此解答即可;
(5)硫代硫酸钠易溶于水,难溶于乙醇,据此选择的洗涤试剂为乙醇;
(6)在洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物,防止沉淀溶解而造成损失;由于装置中存在压强差,所以为了检验洗涤是否完全,应拔下吸滤瓶与安全瓶之间橡皮管,从吸滤瓶上口倒出少量滤液于试管中进行相关实验,据此解答即可;
(7)根据溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
A.滴定管末用Na2S2O3溶液润洗,则Na2S2O3溶液会被稀释;
B.滴定终点时俯视读数,使Na2S2O3溶液体积偏小;
C.锥形瓶用蒸馏水润洗,对实验结果没影响;
D.滴定管尖嘴处滴定前有气泡滴定后气泡消失,体积偏大.
解答 解:(1)由装置图可知a装置为蒸馏烧瓶;故答案为:蒸馏烧瓶;
(2)Na2S2O3在酸性条件下会生成S和二氧化硫,产率会下降,其反应的离子方程式为:S2O32-+2H+=S↓+H2O+SO2↑,故答案为:D;
(3)装置中氢氧化钠是吸收尾气的主要作用,因为原料气二氧化硫是污染性气体不能排放到空气中,以防止污染空气;故答案为:吸收未反应的SO2、H2S等酸性气体;
(4)由题给信息得知:硫代硫酸钠加热易分解,蒸干会使硫代硫酸钠脱水分解,由于溶液表面的温度较低,故晶膜通常在溶液表面出现,故答案为:蒸干会使硫代硫酸钠脱水并分解;因为溶液表面温度较低;
(5)硫代硫酸钠易溶于水,难溶于乙醇,据此选择的洗涤试剂为乙醇,乙醇的结构式为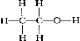 ,故答案为:
,故答案为: ;
;
(6)在洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物,防止沉淀溶解而造成损失;
C、由于装置中存在压强差,所以为了检验洗涤是否完全,应拔下吸滤瓶与安全瓶之间橡皮管,从吸滤瓶上口倒出少量滤液于试管中进行相关实验,
故选A、B、D;
(7)滴定时,液由蓝色恰好变成无色,且半分钟不恢复,可说明达到滴定终点;
A.滴定管末用Na2S2O3溶液润洗,则Na2S2O3溶液会被稀释,所以测出硫代硫酸钠的质量偏小,故纯度偏小,故A正确;
B.滴定终点时俯视读数,使Na2S2O3溶液体积偏小,计算出的硫代硫酸钠的质量偏大,故纯度偏大,故B错误;
C.锥形瓶用蒸馏水润洗,对实验结果没影响,纯度不变,故C错误;
D.滴定管尖嘴处滴定前有气泡滴定后气泡消失,体积偏大小,计算出原溶液中的硫代硫酸钠的质量偏大,则纯度偏大,故D错误;
故答案为:溶液由蓝色恰好变成无色,且半分钟不恢复;A.
点评 本题通过制取Na2S2O3•5H2O的实验操作,考查了物质制备方案的设计、基本实验操作、物质纯度的计算、滴定误差分析等,题目难度中等,明确实验操作与设计及相关物质的性质是解答本题的关键,试题充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

 轻松暑假总复习系列答案
轻松暑假总复习系列答案| A. | F、O、N非金属性依次减弱,HF、H2O、NH3沸点依次降低 | |
| B. | Li、Na、K、Rb、Cs的失电子能力逐渐增强 | |
| C. | Al3+、Mg2+、Na+的离子半径依次增大 | |
| D. | HF、HCl、HBr、HI稳定性依次减弱,还原性依次增强 |
①CS2+3Cl2 $\stackrel{111-140℃}{→}$ CCl4+S2Cl2;②2S+Cl2 $\stackrel{95-100℃}{→}$ S2Cl2.
已知S2Cl2中硫元素显+1价,电子式:
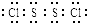 ,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).反应涉及的几种物质的熔沸点如下:
,它不稳定,在水中易发生岐化反应(一部分硫元素价态升高,一部分降低).反应涉及的几种物质的熔沸点如下:| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |

回答下列问题:
(1)装置B、C中玻璃容器的名称:广口瓶;反应原理(填写数字序号):①.
(2)实验中盐酸试剂通常采用36.5%的浓溶液,不用稀盐酸的理由是稀盐酸还原性弱,反应困难.
(3)D中冷凝管起到导气和冷凝双重作用,其冷却水流动方向与热气流流动方向相同(见图).这种冷却方式可应用于下列高中化学中BD实验.
A.石油分馏 B.制取溴苯 C.制取乙酸乙酯 D.制备阿司匹林
(4)B装置中盛放的是饱和食盐水,反应结束后从锥形瓶内混合物中分离出产品的方法是蒸馏,D中采用热水浴加热的原因是使CS2平稳汽化,避免产物S2Cl2汽化.
(5)A部分仪器装配时,放好铁架台后,应先固定酒精灯(填仪器名称),整套装置装配完毕后,应先进行气密性检查再添加试剂.实验完毕,A中不再产生氯气时,可拆除装置.拆除时,最先的操作应当是将E中长导管移开液面.
(6)实验过程中,若缺少C装置,则发现产品浑浊不清,出现该现象的原因可用化学方程式表示为2S2Cl2+2H2O=3S↓+SO2↑+4HCl↑.实验完毕,当把剩余浓盐酸倒入E烧杯中与吸收了尾气的氢氧化钠溶液混合时,发现有少量黄绿色刺激性气体产生,产生该现象的原因是:ClO-+2H++Cl-=Cl2↑+H2O(用离子方程式表示).
| A. | 氨气能使湿润的蓝色石蕊试纸变为红色 | |
| B. | N2中有少量的杂质CO,可将混合气体通过灼热的氧化铜除去CO | |
| C. | 200mL3mol.L-1BaCl2溶液跟100mL3mol.L-1KCl溶液混合后,溶液中c(Cl-)仍然是3 mol/L | |
| D. | 溶液、浊液、胶体的本质区别是粒子直径的大小不同 |
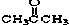 ③CH3CH2Br④
③CH3CH2Br④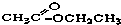 ⑤
⑤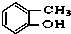 ⑥
⑥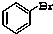
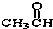 ⑧
⑧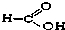 ⑨
⑨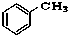 ⑩
⑩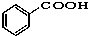

 碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下: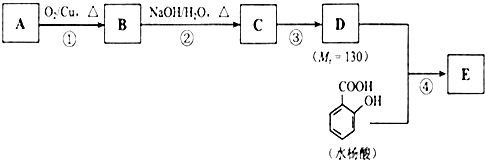
 .
.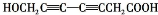 、
、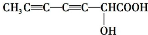 、
、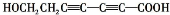 、
、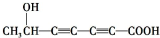 .
.