题目内容
18.CH2=C(CH3)-COOH,它不可能具有的性质是( )| A. | 使酸性高锰酸钾溶液褪色 | B. | 发生加聚反应 | ||
| C. | 与银氨溶液反应 | D. | 与纯碱反应 |
分析 该分子中含有碳碳双键和羧基,所以具有烯烃和羧酸的性质,能发生氧化反应、加成反应、加聚反应、还原反应、取代反应、酯化反应、中和反应,据此分析解答.
解答 解:A.该分子中含有碳碳双键,所以能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故A不选;
B.含有碳碳双键而能发生加聚反应,故B不选;
C.不含醛基,所以不能和银氨溶液发生银镜反应,故C选;
D.含有羧基,所以能和纯碱反应生成二氧化碳、水,故D不选;
故选C.
点评 本题考查有机物结构和性质,明确官能团及其性质关系即可解答,侧重考查烯烃和羧酸性质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.图表示的是某物质所发生的( )


| A. | 置换反应 | B. | 电离过程 | C. | 中和反应 | D. | 水解反应 |
9.关于化学反应速率的说法正确的是( )
| A. | 化学反应速率可表示可逆反应进行的程度 | |
| B. | 化学反应速率是指一定时间内,任何一种反应物浓度的减少或任何一种生成物浓度的增加 | |
| C. | 对于任何化学反应来说,反应速率越快,反应现象就越明显 | |
| D. | 根据反应速率的大小可知化学反应进行的相对快慢 |
6.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是( )
| A. | W、Y、Z的电负性大小顺序一定是Z>Y>W | |
| B. | W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z | |
| C. | Y、Z形成的分子的空间构型可能是正四面体 | |
| D. | 若有WY2,则WY2分子中σ键与π键的数目之比是2:1 |
13.化学与工农业生产和人类生活密切相关.下列说法中,正确的是( )
| A. | 光导纤维、聚酯纤维、棉花都属于高分子化合物 | |
| B. | 在大米酿酒的过程中,淀粉最后变成了单糖 | |
| C. | 泡沫灭火器中用的是苏打和硫酸铝 | |
| D. | 海轮外壳上镶入锌块,可减缓船体的腐蚀 |
10.M+N=Y+Z为吸热反应,对这个反应的下列说法中正确的是( )
| A. | X的能量一定低于M的,Y的能量一定低于N的 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | Z和Y的总能量一定高于M和N的总能量 |
7.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).
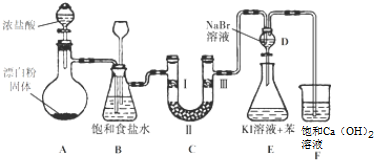
(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是分液漏斗,请写出该反应相应的离子方程式:ClO-+2H++Cl-=Cl2↑++H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是d(填字母编号).
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性.反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是E中溶液分为两层,上层(苯层)为紫红色,该现象不能(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是氯气具有强氧化性,过量的氯气能够将碘离子氧化成碘单质,离子方程式为:Cl2+2I-=I2+2Cl-(用必要的文字和离子方程式回答).
(5)此装置需要改进之处是:F原因是:氢氧化钙为微溶物,溶液中所含溶质较少,吸收氯气不充分,应改为氢氧化钠溶液吸收.

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是分液漏斗,请写出该反应相应的离子方程式:ClO-+2H++Cl-=Cl2↑++H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是d(填字母编号).
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)此装置需要改进之处是:F原因是:氢氧化钙为微溶物,溶液中所含溶质较少,吸收氯气不充分,应改为氢氧化钠溶液吸收.
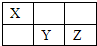 X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示.已知X、Y、Z三元素的质子数之和为40,请回答:
X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示.已知X、Y、Z三元素的质子数之和为40,请回答: