题目内容
【题目】某课外活动小组用下图装置进行实验,K接N,试回答:
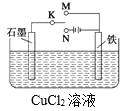
(1)石墨极为______极(填“正”、“负”、“阳” 或“阴”),铁极上的电极反应为:_______。电池总反应为:________。Cu2+向____(填“石墨”或“铁”)电极移动。
(2)若反应过程中有0.1mol的电子发生转移,则铁电极上产生物质的质量为____g,石墨极上产生的物质的物质的量为________mol。
【答案】阳 Cu2++2e- = Cu CuCl2 ![]() Cu + Cl2 铁 3.2 0.05
Cu + Cl2 铁 3.2 0.05
【解析】
(1)K接N,则构成电解池,据此分析;
(2)根据反应CuCl2 ![]() Cu + Cl2计算。
Cu + Cl2计算。
(1)K接N,则构成电解池,此时石墨与电源正极相连,为阳极,铁为阴极,电解氯化铜溶液的总化学方程式为CuCl2![]() Cu+Cl2↑,其中铁极上发生的电极反应为:Cu2++2e-==Cu,Cu2+向铁电极移动,故答案为:阳;Cu2++2e- = Cu;CuCl2
Cu+Cl2↑,其中铁极上发生的电极反应为:Cu2++2e-==Cu,Cu2+向铁电极移动,故答案为:阳;Cu2++2e- = Cu;CuCl2 ![]() Cu + Cl2;铁;
Cu + Cl2;铁;
(2)若反应过程中有0.1mol的电子发生转移,根据反应CuCl2 ![]() Cu + Cl2,则铁电极上析出铜0.05mol,质量为0.05mol×64g/mol= 3.2g,石墨极上产生0.05mol氯气,故答案为:3.2;0.05。
Cu + Cl2,则铁电极上析出铜0.05mol,质量为0.05mol×64g/mol= 3.2g,石墨极上产生0.05mol氯气,故答案为:3.2;0.05。

练习册系列答案
相关题目