题目内容
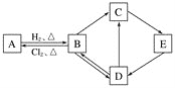
【题目】下图中的每一方格表示相关的一种反应物或生成物。其中B是一种单质,其余物质也都是含有B元素的化合物。C是一种钠盐,E是C对应的酸,B的结构类似金刚石,D为氧化物。
请回答下列问题:
(1)A、D、E的化学式分别为________、________、________。
(2)A和B的互相转化在工业上有什么实际意义?_____________________。
(3)写出D→C反应的化学方程式:_____________________。
(4)写出E→D反应的化学方程式:_____________________。
【答案】SiCl4 SiO2 H2SiO3 粗硅提纯 SiO2+2NaOH=Na2SiO3+H2O H2SiO3![]() SiO2+H2O
SiO2+H2O
【解析】
B是一种单质,其余物质都是含有B元素的化合物,B的结构类似金刚石,则B属于原子晶体,结合转化关系可以知道B为Si元素,而D为B的氧化物,则D是SiO2,A为 SiCl4,C是一种钠盐,则C是Na2SiO3,E是C对应的酸,则E是H2SiO3,结合对应物质的性质以及题目要求解答该题。
B是一种单质,其余物质都是含有B元素的化合物,B的结构类似金刚石,则B属于原子晶体,结合转化关系可以知道B为Si元素,而D为B的氧化物,则D是SiO2,A为 SiCl4,C是一种钠盐,则C是Na2SiO3,E是C对应的酸,则E是H2SiO3,
(1)由以上分析可以知道A为SiCl4,D为SiO2,E为H2SiO3;
因此,本题正确答案是: SiCl4 ,SiO2,H2SiO3。
(2)四氯化硅与氢气反应生成硅和氯化氢,硅与氯气反应生成四氯化硅,因此A和B的互变实际意义是粗硅提纯;
因此,本题正确答案是:粗硅提纯;
(3)二氧化硅和NaOH溶液反应生成硅酸钠,方程式为SiO2+2NaOH=Na2SiO3+H2O;
因此,本题正确答案是: SiO2+2NaOH=Na2SiO3+H2O。
(4) H2SiO3不稳定,加热分解可生成SiO2,方程式为H2SiO3![]() SiO2+H2O;
SiO2+H2O;
因此,本题正确答案是: H2SiO3![]() SiO2+H2O。
SiO2+H2O。

【题目】工业上用含三价钒(V2O3)为主的某石煤为原料(含有Al2O3、CaO等杂质),钙化法焙烧制备V2O5,其流程如下:
![]()
【资料】:+5价钒在溶液中的主要存在形式与溶液pH的关系:
pH | 4~6 | 6~8 | 8~10 | 10~12 |
主要离子 | VO2+ | VO3 | V2O74 | VO43 |
(1)焙烧:向石煤中加生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式是______。
(2)酸浸: ① Ca(VO3)2难溶于水,可溶于盐酸。若焙砂酸浸时溶液的pH=4,Ca(VO3)2溶于盐酸的离子方程式是______。
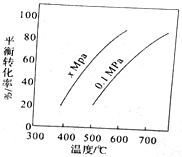
② 酸度对钒和铝的溶解量的影响如图所示:酸浸时溶液的酸度控制在大约3.2%,根据如图推测,酸浸时不选择更高酸度的原因是______。

(3)转沉:将浸出液中的钒转化为NH4VO3固体,其流程如下:
![]()
① 浸出液中加入石灰乳的作用是______。
② 已知CaCO3的溶解度小于Ca3(VO4)2。向Ca3(VO4)2沉淀中加入(NH4)2CO3溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:______。
③ 向(NH4)3VO4溶液中加入NH4Cl溶液,控制溶液的pH=7.5。当pH>8时,NH4VO3的产量明显降低,原因是______。
(4)测定产品中V2O5的纯度:
称取a g产品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入b1 mL c1 mol·L1 (NH4)2Fe(SO4)2溶液(VO2+ + 2H+ + Fe2+ == VO2+ + Fe3+ + H2O)。最后用c2 mol·L1 KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2 mL。已知 MnO4被还原为Mn2+,假设杂质不参与反应。则产品中V2O5的质量分数是______。(V2O5的摩尔质量:182 g·mol1)
【题目】纳米级Fe3O4呈黑色,因其有磁性且粒度小而在磁记录材料、生物功能材料等诸多领域有重要应用,探究其制备和用途意义重大。
(1)还原-沉淀法:①用还原剂Na2SO3将一定量Fe3+可溶盐溶液中的1/3Fe3+还原,使Fe2+和Fe3+的物质的量比为1:2。②然后在①所得体系中加入氨水,铁元素完全沉淀形成纳米Fe3O4。写出②过程的离子方程式:__________________________。
当还原后溶液中c(Fe2+):c(Fe3+)=2:1时,由下表数据可知,产品磁性最大,可能的原因是___________________________ 。
c(Fe2+):c(Fe3+) | 沉淀性状 | 磁性大小 |
1:3 | 红棕色 | 92.7% |
1:2 | 棕色 | 96.5% |
2:1 | 黑色 | 100% |
(2)电化学法也可制备纳米级Fe3O4,用面积为4cm2的不锈钢小球(不含镍、铬)为工作电极,铂丝作阴极,用Na2SO4溶液作为电解液,电解液的pH维持在10左右,电流50mA。生成Fe3O4的电极反应为________________________。
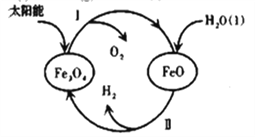
(3)已知:H2O(l)=H2(g)+1/2O2(g) △H=+285.5kJ·mol-1,以太阳能为热源分解Fe3O4,经由热化学铁氧化合物循环分解水制H2的过程如下,完善以下过程Ⅰ的热化学方程式。
过程Ⅰ:________________________________,
过程Ⅱ:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) △H=+128.9kJ·mol-1
(4)磁铁矿(Fe3O4)常作冶铁的原料,主要反应为:Fe3O4(s)+4CO(g)![]() 3Fe(s)+4CO2(g),该反应的△H<0,T℃时,在IL恒容密闭容器中,加入Fe3O4、CO各0.5mol,10min后反应达到平衡时,容器中CO2的浓度是0.4mol·L-1。
3Fe(s)+4CO2(g),该反应的△H<0,T℃时,在IL恒容密闭容器中,加入Fe3O4、CO各0.5mol,10min后反应达到平衡时,容器中CO2的浓度是0.4mol·L-1。
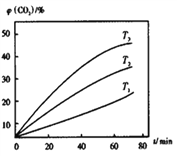
①T℃时,10min内用Fe3O4表示的平均反应速率为_____g·min-1。
②其他条件不变时,该反应在不同温度下,CO2含量随时间的变化φ(CO2)-t曲线如图所示,温度T1、T2、T3由大到小的关系是_________________,判断依据是___________________。