题目内容
α-AgI是一种固体导体,导电率很高。为研究α-AgI到底是Ag+导电还是I—导电,设计了如下实验,下列有关说法不正确的是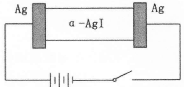
| A.若α-AgI是Ag+导电,则通电一段时间后晶体质量不变 |
| B.若α-AgI是Ag+导电,则通电一段时间后晶体质量减少 |
| C.阳极反应为:Ag一e—=Ag+ |
| D.阴极质量不断增加 |
B
解析试题分析:若α-AgI是Ag+导电,阳极反应式为Ag一e—=Ag+,阳极质量减小;内电路中Ag+移向阴极,阴极反应式为Ag++e—=Ag,阴极质量增大;由电子守恒可知,阳极减小的质量等于阴极增加的质量,则α-AgI晶体的质量不变。
考点:考查电解原理的应用等相关知识。

练习册系列答案
相关题目
如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加一滴石蕊溶液。下列实验现象中错误的是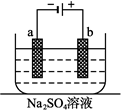
| A.a电极附近呈红色,b电极附近呈蓝色 |
| B.a电极附近呈蓝色,b电极附近呈红色 |
| C.逸出气体的体积,a电极的大于b电极的 |
| D.a、b两电极都逸出无色无味气体 |
利用如图所示装置可以模拟铁的电化学防护。下列说法不正确的是 ( )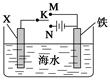
| A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀 |
| B.若X为锌棒,开关K置于M处,铁极发生氧化反应 |
| C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀 |
| D.若X为碳棒,开关K置于N处,X极发生氧化反应 |
下列关于金属腐蚀与防护的说法错误的是
| A.当镀锡铁制品的镀层破损时,镀层不再对铁制品起保护作用 |
| B.在空气与水面交接处的钢柱,比在水下部分的钢柱容易腐蚀 |
| C.钢铁不论发生析氢腐蚀还时吸氧腐蚀,其负极反应都为Fe-2e-=Fe2+ |
| D.将输油管道与电源的正极相连的防护方法叫做牺牲阳极的阴极保护法 |
铜板上铁铆钉处的腐蚀原理如图所示,下列有关说法中正确的是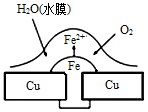
| A.此过程中铜被腐蚀 |
| B.此过程中电子从Cu移向Fe |
| C.正极电极反应式为O2+2H2O+4e-=4OH- |
| D.铁钉表面发生的反应为Fe-3e- ═ Fe3+ |
某些食品包装盒中有一个小袋,袋上注明“双吸剂,不可食用”,通过上网查询得知其主要成分是铁粉、活性炭和氯化钠”。关于这种双吸剂的分析判断错误的是
| A.具有抗氧化作用 | B.可吸收食品盒内的O2和N2 |
| C.发挥作用时利用了原电池原理 | D.变为红褐色后失效 |
有关电化学原理的推断正确的是
| A.金属腐蚀就是金属原子失去电子被还原的过程 |
| B.钢铁吸氧腐蚀时,负极反应式为:2H2O+O2+4e→4OH- |
| C.氯碱工业中,阳极发生的反应为:2Cl-–2e→Cl2↑ |
| D.镀锌铁皮的镀层损坏后,铁更容易腐蚀 |
银制器皿表面日久因生成Ag2S而变黑,可进行如下处理:将表面发黑的银器浸入盛有食盐水的铝质容器中(如图),一段时间后黑色褪去。有关说法正确的是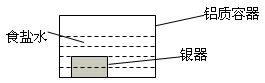
| A.该处理过程中电能转化为化学能 |
| B.银器为正极,Ag2S还原为单质银 |
| C.Ag2S溶解于食盐水生成了AgCl |
| D.铝质容器为阳极,其质量变轻 |
下图为一原电池装置,下列叙述中正确的是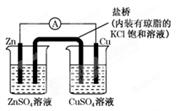
| A.铜是阳极,铜片上有气泡产生 |
| B.盐桥中的K+ 移向ZnSO4溶液 |
| C.电流从锌片经导线流向铜片 |
| D.铜离子在铜片表面被还原 |