题目内容
利用如图所示装置可以模拟铁的电化学防护。下列说法不正确的是 ( )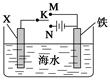
| A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀 |
| B.若X为锌棒,开关K置于M处,铁极发生氧化反应 |
| C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀 |
| D.若X为碳棒,开关K置于N处,X极发生氧化反应 |
B
解析试题分析:A.若开关K置于M处,为原电池,由于活动性Zn>Fe,所以锌棒作负极,首先被氧化而腐蚀,对铁起到了保护作用,故可减缓铁的腐蚀。正确不符合题意。B.若开关K置于M处. 为原电池,由于活动性Zn>Fe,所以锌棒作负极发生氧化反应,,铁极作正极,正极上发生还原反应。错误,符合题意。若开关K置于N处该装置为电解池。由于阳极X为碳棒,是惰性电极,溶液中的Cl-在该电极上失去电子,发生氧化反应。在阴极Fe上,H+得到电子,发生还原反应,产生氢气。对铁来说未被腐蚀,因此被保护可减缓铁的腐蚀C.D正确不符合题意。
考点:考查铁的电化学防护的知识。

练习册系列答案
相关题目
用惰性电极分别电解下列各物质的水溶液一段时间后,向剩余溶液中加入适量水能使溶液恢复到电解前浓度的是
| A.CuSO4 | B.Na2SO4 | C.CuCl2 | D.NaCl |
为充分利用海洋资源,研究人员发明海水电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl
下列说法错误的是
| A.负极反应式: Ag+Cl――e-=AgCl |
| B.每生成1 mol Na2Mn5O10转移2 mol电子 |
| C.Cl―不断向电池的正极移动 |
| D.Na2Mn5O10是还原产物 |
电池在生产、生活中应用越来越广泛。下列说法错误的是
| A.化学电源有一次电池、可充电电池和燃料电池等,一次电池只能放电,不能充电 |
| B.铅蓄电池应用广泛,主要优点是单位重量的电极材料释放的电能大 |
| C.燃料电池具有能量利用率高、可连续使用和污染轻等优点 |
| D.锂电池是一种高能电池,体积小、重量轻,单位质量能量比高 |
下列有关金属腐蚀与防护的说法中正确的是
| A.在生产生活中比较普遍而且危害较大的是金属的化学腐蚀 |
| B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
α-AgI是一种固体导体,导电率很高。为研究α-AgI到底是Ag+导电还是I—导电,设计了如下实验,下列有关说法不正确的是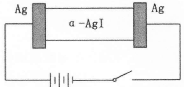
| A.若α-AgI是Ag+导电,则通电一段时间后晶体质量不变 |
| B.若α-AgI是Ag+导电,则通电一段时间后晶体质量减少 |
| C.阳极反应为:Ag一e—=Ag+ |
| D.阴极质量不断增加 |
体积为1 L的某溶液中含有的离子如表所示:
| 离子 | Cu2+ | Al3+ | NO3— | Cl- |
| 物质的量浓度 mol/L | 1 | 1 | a | 1 |
用Pt电极电解该溶液,当电路中有3 mol电子通过时(忽略电解时溶液体积的变化及电解产物可能存在的溶解现象),下列说法正确的是 ( )。
A.电解后溶液的pH=0
B.a=3
C.阳极生成1.5 mol Cl2
D.阴极析出的金属是铜与铝
 从右向左移动。下列分析正确的是
从右向左移动。下列分析正确的是