题目内容
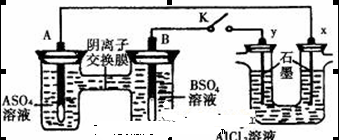
有关电化学原理的推断正确的是
| A.金属腐蚀就是金属原子失去电子被还原的过程 |
| B.钢铁吸氧腐蚀时,负极反应式为:2H2O+O2+4e→4OH- |
| C.氯碱工业中,阳极发生的反应为:2Cl-–2e→Cl2↑ |
| D.镀锌铁皮的镀层损坏后,铁更容易腐蚀 |
C
解析试题分析:A.金属腐蚀是金属原子失去电子被氧化的过程,错误。B.钢铁吸氧腐蚀时,正反应式为:2H2O+O2+4e→4OH-,错误。C.阳极是失电子的反应,发生的反应为:2Cl-–2e→Cl2↑,正确。D.镀锌铁皮的镀层损坏后,形成原电池时锌做负极仍会对铁起到保护作用,错误。
考点:本题主要考查电化学原理的运用。

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案
相关题目
用惰性电极分别电解下列各物质的水溶液一段时间后,向剩余溶液中加入适量水能使溶液恢复到电解前浓度的是
| A.CuSO4 | B.Na2SO4 | C.CuCl2 | D.NaCl |
α-AgI是一种固体导体,导电率很高。为研究α-AgI到底是Ag+导电还是I—导电,设计了如下实验,下列有关说法不正确的是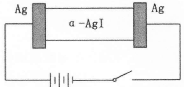
| A.若α-AgI是Ag+导电,则通电一段时间后晶体质量不变 |
| B.若α-AgI是Ag+导电,则通电一段时间后晶体质量减少 |
| C.阳极反应为:Ag一e—=Ag+ |
| D.阴极质量不断增加 |
某小组为研究电化学原理,设计如图装置。下列叙述错误的是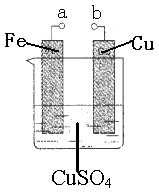
| A.a和b不连接时,铁片质量会增加 |
| B.a和b用导线连接时,正极发生的电极反应为:Cu2++2e-=Cu |
| C.无论a和b是否连接,铁片均被腐蚀 |
| D.a和b分别连接电源正、负极时,Fe电极发生的电极反应为:4OH--4e-=2H2O+O2↑ |
一定条件下,碳钢腐蚀与溶液pH的关系如下:
| pH | 2 | 4 | 6 | 6.5 | 8 | 13.5 | 14 | |
| 腐蚀快慢 | 较快 | 慢 | 较快 | |||||
| 主要产物 | Fe2+ | Fe3O4 | Fe2O3 | FeO2- | ||||
下列说法不正确的是
A.在pH<4的溶液中,碳钢主要发生析氢腐蚀
B.在pH>6的溶液中,碳钢主要发生吸氧腐蚀
C.在pH>14的溶液中,碳钢腐蚀的正极反应为O2+4OH-+4e-=2H2O
D.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减慢
下列有关用惰性电极电解AgNO3溶液的说法不正确的是:
| A.电解过程中阴极质量不断增大 |
| B.电解过程中阳极附近的pH不断降低 |
| C.电解一段时间后,向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况 |
| D.电解过程中,溶液中电子由阴极迁向阳极 |
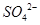 从右向左移动。下列分析正确的是
从右向左移动。下列分析正确的是