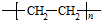题目内容
14.0.2mol某烷烃完全燃烧后,将生成的气体通入0.5L 2mol/L NaOH溶液中,生成的Na2CO3和NaHCO3的物质的量之比为1:3,则该烷烃为( )| A. | 甲烷 | B. | 乙烷 | C. | 丙烷 | D. | 丁烷 |
分析 根据氢氧化钠中钠元素的物质的量和碳酸钠、碳酸氢钠中钠元素的总物质的量相等,据此可以确定碳元素的量以及个数,并得出烷烃的氢原子数目,确定烷烃.
解答 解:因生成物中Na2CO3、NaHCO3共存,故烷烃完全燃烧产生的CO2与NaOH完全反应.
n(NaOH)=2mol•L-1×0.5L=1mol
n(Na2CO3)=$\frac{1}{5}$×1mol=0.2mol
n(NaHCO3)=$\frac{3}{5}$×1mol=0.6mol
总碳量(即CO2的物质的量)为:0.2mol+0.6mol=0.8mol
1mol烷烃中含C的物质的量为$\frac{0.8mol}{0.2mol}$×1mol=4mol,因此该烃为丁烷,故选D.
点评 本题考查烃燃烧的有关计算,难度中等,可以根据方程式计算,本题采取守恒计算,简化计算,注意守恒思想在计算中的运用

练习册系列答案
相关题目
4.在NH4Cl饱和溶液中分别加入①Mg;②NH4Cl(固);③NH4HCO3;④H2O;⑤氯水;⑥Cu.能使该溶液的pH值增大的是( )
| A. | ②③ | B. | ①②⑤ | C. | ②③⑥ | D. | ①③④ |
5. 丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如图所示,下列说法不正确的是( )
丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如图所示,下列说法不正确的是( )
 丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如图所示,下列说法不正确的是( )
丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如图所示,下列说法不正确的是( )| A. | 萨罗的分子式为C13H10O3 | |
| B. | 丁子香酚和萨罗均能与氯化铁溶液发生显色反应 | |
| C. | 丁子香酚与浓溴水只发生取代反应 | |
| D. | 萨罗和丁子香酚均能发生氧化反应 |
2.用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊.再升高至65℃以上,溶液变澄清. | C6H5ONa溶液 |
| B | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失. | Na2AlO2溶液 |
| C | 通入CO2,溶液变浑浊.再加入品红溶液,红色褪去. | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊. | Ca(OH)2溶液 |
| A. | A | B. | B | C. | C | D. | D |
9.已知某温度下CuSO4的溶解度为25g,取该温度下的饱和溶液200g,再加入16gCuSO4固体,则溶液中析出晶体的质量约为( )
| A. | 4g | B. | 25g | C. | 29g | D. | 30g |
19.A、B两种原子,A原子M层比B原子M层少3个电子,B原子L层电子数恰好是A原子L层的两倍,则A元素是( )
| A. | O | B. | Si | C. | C | D. | Mg |
6.下列互为同位素的一组是( )
| A. | 金刚石和石墨 | B. | mnX和wnX | ||
| C. | 质子数相同、中子数不同的微粒 | D. | 11H和21H |

 .
.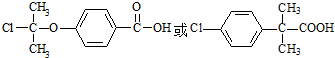 .
. (R、R′为烃基).根据已有知识并结合相关信息,写出以乙醇为原料制备
(R、R′为烃基).根据已有知识并结合相关信息,写出以乙醇为原料制备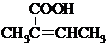 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: