题目内容
【题目】室温时将100mLH2S和O2的混合气体,点燃完全反应后恢复到原来状况,体积变为40mL。下列叙述中正确的是( )
A.剩余40mL气体一定是O2
B.剩余40mL气体是H2S或SO2
C.混合气体中含H2S40mL或80mL
D.剩余40mL气体是SO2和O2混合气体
【答案】BC
【解析】
H2S和O2的混合气体点燃,氧气不足量时发生反应①2H2S+O2═2S↓+2H2O,氧气足量时发生反应②2H2S+3O2═2SO2+2H2O。若n(H2S):n(O2)≥2:1,发生反应①,H2S刚好完全反应或有剩余;若n(H2S):n(O2)≤2:3,发生反应②,氧气可能有剩余,气体为二氧化硫(可能含有氧气);若2:3<n(H2S) :n(O2)<2:1,发生反应①②,气体为二氧化硫。
A.若O2有剩余,则剩余40mL气体一定含有SO2,A不合题意;
B.若剩余40mL气体是H2S,则参加反应的H2S、O2为60mL,且只发生反应①2H2S+O2═2S↓+2H2O;若剩余40mL气体是SO2,则参加反应的H2S、O2为100mL,且只发生反应②2H2S+3O2═2SO2+2H2O,V(H2S)=![]() ×100mL=40mL=V(SO2),B符合题意;
×100mL=40mL=V(SO2),B符合题意;
C.若混合气体中含H2S40mL,则含O260mL,刚好发生反应②2H2S+3O2═2SO2+2H2O,生成V(SO2)=40mL;若混合气体中含H2S 80mL,则含O220mL,只发生反应①2H2S+O2═2S↓+2H2O,消耗H2S40mL,剩余40mL,C符合题意;
D.剩余40mL气体是SO2和O2混合气体,设剩余O2的体积为x,则生成SO2的体积为40-x,参加反应的H2S、O2为100-x,只发生反应②2H2S+3O2═2SO2+2H2O,V(H2S)=![]() ×(100-x),依据SO2的体积相等可得:
×(100-x),依据SO2的体积相等可得:![]() ×(100-x)=40-x,x=0,D 不合题意;
×(100-x)=40-x,x=0,D 不合题意;
故选BC。

 全能测控期末小状元系列答案
全能测控期末小状元系列答案【题目】1-乙氧基萘常用作香料,也可合成其他香料。实验室制备1-乙氧基萘的过程如下:
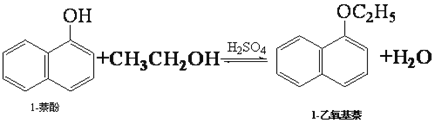
已知:1-萘酚的性质与苯酚相似,有难闻的苯酚气味。相关物质的物理常数:
物质 | 相对分子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度 | |
水 | 乙醇 | |||||
1-萘酚 | 144 | 无色或黄色菱形结晶或粉末 | 96℃ | 278℃ | 微溶于水 | 易溶于乙醇 |
1-乙氧基萘 | 172 | 无色液体 | 5.5℃ | 267℃ | 不溶于水 | 易溶于乙醇 |
乙醇 | 46 | 无色液体 | -114.1℃ | 78.5℃ | 任意比混溶 | |
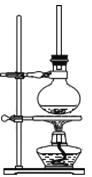
(1)将72g 1-萘酚溶于100mL无水乙醇中,加入5mL浓硫酸混合。将混合液置于如图所示的容器中加热充分反应。实验中使用过量乙醇的原因是________。
(2)装置中长玻璃管的作用是:______________。
(3)该反应能否用实验室制备乙酸乙酯的装置_____(选填“能”或“不能”),简述理由_____________。
(4)反应结束,将烧瓶中的液体倒入冷水中,经处理得到有机层。为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液碱洗并分液;④用无水氯化钙干燥并过滤。正确的顺序是____________(选填编号)。
a.③②④① b.①②③④ c.②①③④
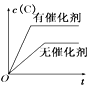
(5)实验测得1-乙氧基萘的产量与反应时间、温度的变化如图所示,时间延长、温度升高,1-乙氧基萘的产量下降可能的两个原因是____________。

(6)提纯的产品经测定为43g,本实验中1-乙氧基萘的产率为________。