题目内容
【题目】下列叙述正确的是
A.恒容密闭容器中进行的反应3A(g)![]() B(g)+C(g),在其它条件不变情况下,再充入一定量的A气体,A的转化率将增大
B(g)+C(g),在其它条件不变情况下,再充入一定量的A气体,A的转化率将增大
B.对于可逆反应N2(g)+3H2(g)![]() 2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增加
2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增加
C.将AlCl3溶液和NaAlO2溶液分别蒸干后灼烧,所得固体产物均为Al2O3
D.反应NH3(g)+HCl(g)=NH4Cl(s)△H<0在任何条件下均能自发进行
【答案】A
【解析】
A.该反应正反应方向气体的系数减小,在其他条件不变的情况下,再充入一定量的A气体,容器内压强增大,平衡向右移动, A的转化率将增大,A正确;
B.增大氮气浓度可增加活化分子的数目,但不能增加活化分子百分数,B错误;
C.将A1C13溶液蒸干后灼烧,所得固体产物为Al2O3,将NaAlO2溶液蒸干后灼烧所得固体物质为NaAlO2,C错误;
D.反应NH3(g)+HCl(g)=NH4C1(s) ΔH<0,S < 0,H-TS高温时可能> 0,不能自发进行,D错误;
答案选A。

 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
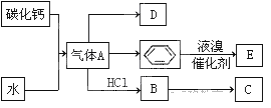
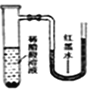
(1)氨气的制备

①氨气的发生装置可以选择上图中的________,反应的化学方程式为______________。
②预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→______(按气流方向,用小写字母表示)。
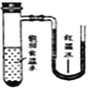
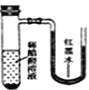
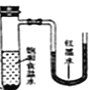
(2)氨气与二氧化氮的反应将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中_____________ | ②反应的化学方程式 ____________ |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
打开K2 | ③_______________ | ④______________ |
【题目】I. 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色液体,易溶于水。为研究A 的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
①称取9.0gA,升温使其气化,测其密度是相同条件下H2的45 倍 | 试通过计算填空:(1)A的相对分子质量为________ |
②将此9.0gA在足量纯O2中充分 燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g | (2)A的分子式为________ |
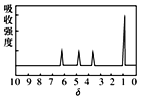
③又知A含有官能团—COOH、—OH,且A的核磁共振氢谱如图: |
|
(3)综上所述,A的结构简式为________ | |
II. 工业上常以A物质为原料合成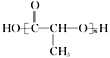 ,该反应类型属于______(填字母代号,下同)反应。
,该反应类型属于______(填字母代号,下同)反应。
A 加聚 B 缩聚
III. 下列关于物质的分离、提纯实验中的一些操作或做法,正确的是_______。
A 在组装蒸骝装置时,温度计的水银球应伸入液面下
B 用96%的工业酒精制取无水乙醇时,先加入无水CuSO4,再过滤
C 在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加入少量蒸馏水
D 在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后要冷却到常温再过滤
【题目】25℃,几种物质的pH和浓度如下表所示。回答下列问题:
序号 | ① | ② | ③ | ④ |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
pH | 11 | 11 | 3 | 3 |
浓度 | c1 | c2 | c3 | c4 |
(1)c1____(填“>”“<”或“=”)c2。
(2)溶液中水的电离程度②____(填“>”“<”或“=”)③。
(3)分别加水稀释10倍,稀释后四种溶液的pH由大到小的顺序为____(填序号)。
(4)①溶液与④溶液等体积混合,溶液的pH____7(填“>”“<“或“=”),用④溶液滴定①溶液,滴定过程中不可能出现的结果是____。
A. c(NH4+)>c(Cl-)>c(OH-)>c(H+)
B. c(NH4+)=c(Cl-)>c(OH-)=c(H+)
C. c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D. c(Cl-)>c(NH4+)>c(H+)>c(OH-)
E. c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(5)氢氧化铜悬浊液中有如下平衡:Cu(OH)2(s)![]() Cu2+(aq)+2OH-(aq),常温下,Ksp=c(Cu2+)·c2(OH-)=2×10-20。某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液使之pH>_____。
Cu2+(aq)+2OH-(aq),常温下,Ksp=c(Cu2+)·c2(OH-)=2×10-20。某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液使之pH>_____。