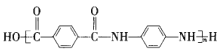��Ŀ����
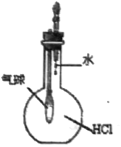
����Ŀ����(Se)�ǵ������ڵ�VIA��Ԫ�أ��������ڲ��ɻ�ȱ����Ԫ�أ�H2Se���Ʊ������̫���ܵ�ء��뵼����Ϻͽ������������Ҫԭ�ϡ�
(1)��֪����2H2Se(g)+O2(g)![]() 2Se(s)+2H2O(l) ��H1=akJ/mol
2Se(s)+2H2O(l) ��H1=akJ/mol
��2H2(g)+O2(g)![]() 2H2O(l) ��H2=bkJ��mol-1
2H2O(l) ��H2=bkJ��mol-1
��Ӧ H2(g)+Se(s)![]() H2Se(g) ��H3=___________kJ/mol(�ú�a��b �Ĵ���ʽ����)��
H2Se(g) ��H3=___________kJ/mol(�ú�a��b �Ĵ���ʽ����)��
(2)T��ʱ����һ�����ܱ������м���3molH2��lmolSe��������ӦH2(g)+Se(s)![]() H2Se(g)��
H2Se(g)��
������������жϷ�Ӧ�ﵽƽ��״̬����__________(����ĸ����)��
a.������ܶȲ��� b.v(H2)= v(H2Se)
c.�����ѹǿ���� d.�����ƽ��Ħ����������
�ڵ���Ӧ�ﵽƽ���ƽ�������ͨ������Һ��������ʹH2Se����ת��ΪH2SeҺ�壬����������� H2�ٴ�ͨ�뷢����Ӧ���ܱ������м�����Se��Ӧʱ��Se��ת���ʻ����{�����û�ѧƽ�����۽��ͣ�_____________________________________________��
����5Сʱ�ڵõ���H2SeΪ����ָ�꣬���¶ȡ�ѹǿ��H2Se���ʵ�Ӱ����ͼ��ʾ��
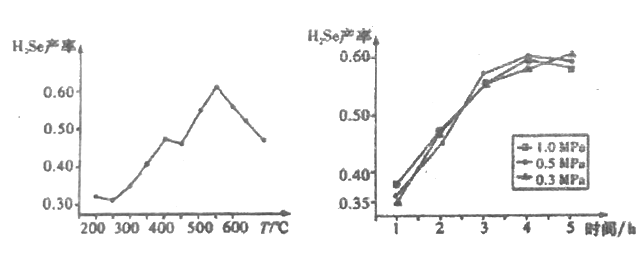
���Ʊ�H2Se����ќضȺ�ѹǿΪ______________________________��
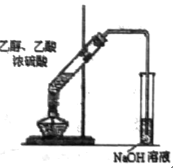
(3)��ҵ�ϴӺ�����������ȡ���ķ�����������������ƵĻ����Һ����������������������ᣬ�������Ṳ�ȣ�����ת��Ϊ�����ᣬ���������ᷴӦ�Ļ�ѧ����ʽΪ_________�����ͨ��SO2���������ʡ�
(4)��֪������H2Se�ĵ���ƽ�ⳣ��K1=1.3��10-4��K2=5.0��10-11����NaHSe��Һ��__________(��������������������)����ͨ����������˵��___________________________��
���𰸡�![]() (b-a) ad �Ƴ�����H2Se���������H2����ͨ�������У� ��ʹƽ�������ƶ���Se��ת�������{ 550�桢0.3MPa
(b-a) ad �Ƴ�����H2Se���������H2����ͨ�������У� ��ʹƽ�������ƶ���Se��ת�������{ 550�桢0.3MPa ![]() ���� HSe-�ĵ��볣��ΪK2=5.0��l0-11��HSe-��ˮ�ⳣ��Ϊ7.7��l0-11���ʵ���С��ˮ�⣬��Һ�ʼ���
���� HSe-�ĵ��볣��ΪK2=5.0��l0-11��HSe-��ˮ�ⳣ��Ϊ7.7��l0-11���ʵ���С��ˮ�⣬��Һ�ʼ���
��������
(1)��֪����2H2Se(g)+O2(g)![]() 2Se(s)+2H2O(l) ��H1=akJ/mol
2Se(s)+2H2O(l) ��H1=akJ/mol
��2H2(g)+O2(g)![]() 2H2O(l) ��H2=bkJ��mol-1
2H2O(l) ��H2=bkJ��mol-1
��˹���ɼ���(��-��)��![]() �õ���ӦH2(g)+Se(s)
�õ���ӦH2(g)+Se(s)![]() H2Se(g)�ķ�Ӧ�ȡ�H��
H2Se(g)�ķ�Ӧ�ȡ�H��
(2)��ƽ��״̬��־�����淴Ӧ������ͬ������ֺ������ֲ��䣬�ݴ˷�����
�ڽ��������H2�ٴ�ͨ�뷢����Ӧ���ܱ������м�����Se��Ӧʱ��������������һ�ֻ������һ��ת���ʣ�
������ͼ��仯���Ʒ����ж���ѷ�Ӧ������
(3)���������Ṳ�ȣ�����ת��Ϊ�����������ӱ�����Ϊ���������ԭ���غ㡢�����غ���д��ѧ����ʽ��
(4)����NaHSe��Һ��ˮ��ƽ�ⳣ�����͵ڶ�������ƽ�ⳣ���Ƚ��ж���Һ����ԣ�
(1)��֪����2H2Se(g)+O2(g)![]() 2Se(s)+2H2O(l) ��H1=akJ/mol
2Se(s)+2H2O(l) ��H1=akJ/mol
��2H2(g)+O2(g)![]() 2H2O(l) ��H2=bkJ��mol-1
2H2O(l) ��H2=bkJ��mol-1
���ݸ�˹���ɣ���(��-��)��![]() �õ���ӦH2(g)+Se(s)
�õ���ӦH2(g)+Se(s)![]() H2Se(g)�ķ�Ӧ�ȡ�H=
H2Se(g)�ķ�Ӧ�ȡ�H= ![]() (b-a)kJ/mol��
(b-a)kJ/mol��
(2)��T��ʱ����һ�����ܱ������м���3molH2��1 mol Se��������ӦH2(g)+Se(s)![]() H2Se(g)��
H2Se(g)��
a.��Ӧǰ�����������仯������������䣬��������ܶȲ���˵����Ӧ�ﵽƽ��״̬��a��ȷ��
b.v(H2)=v(H2Se)δָ����Ӧ������Ӧ���ʻ����淴Ӧ���ʣ���˲���˵�����淴Ӧ������ͬ��b����
c.��Ӧǰ���������ʵ������䣬�����ѹǿʼ�ղ��䣬��˲���˵����Ӧ�ﵽƽ��״̬��c����
d.��Ӧǰ�����������仯�����������ʵ������䣬����������ƽ��Ħ���������䣬˵����Ӧ�ﵽƽ��״̬��d��ȷ��
�ʺ���ѡ����ad��
�ڵ���Ӧ�ﵽƽ���ƽ��������ͨ������Һ��������ʹH2Se����ת��ΪH2SeҺ�壬�����������H2�ٴ�ͨ�뷢����Ӧ���ܱ������м�����Se��Ӧʱ��Se��ת���ʻ���ߣ����������Ƴ�����H2Se�����������������ͨ�������У�ƽ�������ƶ���ʹSe��ת������ߣ�
�۸���ͼʾ��֪�Ʊ�H2Se������¶Ⱥ�ѹǿΪ��550�桢0.3MPa��
(3)���������Ṳ�ȣ�����ת��Ϊ�����ᣬ�����ӱ�����Ϊ���������ԭ���غ㡢�����غ���д��ѧ����ʽ��![]() ��
��
(4)��֪������H2Se�ĵ���ƽ�ⳣ��K1=1.3��10-4��K2=5.0��10-11��NaHSe��Һ�д���ˮ��ƽ��HSe-+H2O![]() H2Se+OH-��Kh=
H2Se+OH-��Kh=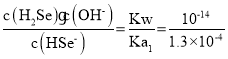 =7.7��10-11��K2=5.0��10-11��ˮ��̶ȴ��������̶ȣ���Һ�Լ��ԣ�
=7.7��10-11��K2=5.0��10-11��ˮ��̶ȴ��������̶ȣ���Һ�Լ��ԣ�

����Ŀ����������ʵ��������������ó��Ľ�����ȷ����
ѡ�� | ʵ����������� | ���� |
A | ��ʢ��ij����Һ���Թ��е�������������Һ���ȣ��Թܿڴ�ʪ��ĺ�ɫʯ����ֽ���� | �����к� |
B | ����ˮ��ͨ��ij��ɫ���壬��ˮ��ɫ | �����������CH2=CH2 |
C | һ������ͭ�������ַ�Ӧ����ͭʣ�࣬�ټ�������ϡ���ᣬͭ�����ܽ⣬�������ݷų� | Cu��ϡ���ᷢ���˷�Ӧ |
D | �������Һ�м�����ϡ���ᣬ����4~5min����ȴ�������м�������Cu(OH)2����Һ�����������ڣ���ש��ɫ���� | ����û�з���ˮ�� |
A.AB.BC.CD.D