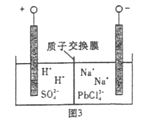
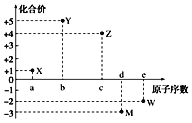
题目内容
【题目】已知氧化性:![]() 。向
。向![]() 溶液中通入一定量的
溶液中通入一定量的![]() ,发生反应的离子方程式为
,发生反应的离子方程式为![]() 。其中x、y、z的值不符合实际反应的是
。其中x、y、z的值不符合实际反应的是
A.![]() B.
B.![]()
C.![]() D.
D.![]()
【答案】B
【解析】
氧化还原反应的离子方程式中满足电子守恒和电荷守恒,![]() 中电子守恒关系式为:x+y=2z、电荷守恒关系式为:2x-y=3x-2z,即关系式均为x+y=2z,将x、y、z的数值代入关系式x+y=2z中检验:
中电子守恒关系式为:x+y=2z、电荷守恒关系式为:2x-y=3x-2z,即关系式均为x+y=2z,将x、y、z的数值代入关系式x+y=2z中检验:
A.x=4、y=6,z=5时,4+6=2×5,所以符合实际反应,故A正确;
B.x=1、y=5,z=1时,1+5>2×1,所以不符合实际反应,该B错误;
C.x=3、y=1、z=2时,3+1=2×2,所以符合实际反应,故C正确;
D.x=2、y=2、z=2,2+2=2×2,所以符合实际反应,故D正确;
故选:B。

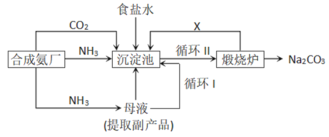
【题目】锰锌铁氧体是应用广泛的高性能磁性材料。现以akg废旧碱性锌锰电池为原料(含锰元素的物质:MnO2占b%,MnOOH占c%)制备锰锌铁氧体,主要流程如下:
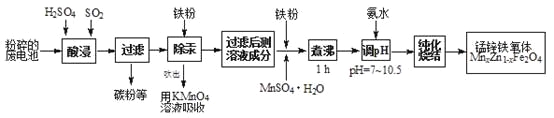
(1)酸浸废电池时,被溶解生成Zn2+的物质有______,SO2的作用是_____(填字母编号)。
A.漂白剂 | B.沉淀剂 | C.氧化剂 | D.还原剂 |
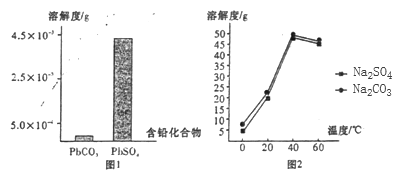
(2)除汞是以氮气为载体吹入滤液带出汞蒸汽,经KMnO4溶液吸收而实现的。如图是KMnO4溶液处于不同pH时对应的单位时间Hg去除率变化图,图中物质为Hg与MnO4-在该pH范围反应的主要产物。
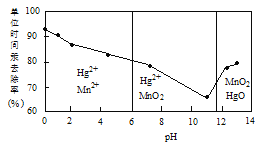
①pH<6时反应的离子方程式为___________。
②汞的去除速率随pH变化的规律是_________。
(3)锌锰干电池中MnO2可以用碳酸锰在空气中煅烧制得。
已知25℃,101 kPa时:2MnO(s)+O2(g)=2MnO2(s) H=-272.0 kJ/mol
MnCO3(s)=MnO(s)+CO2(g) H=+116.6 kJ/mol
碳酸锰在空气中煅烧反应生成MnO2的热化学方程式是_______________。
(4)x=0.2的锰锌铁氧体具有较高的饱和磁场强度,该锰锌铁氧体的组成用氧化物形式(最简整数比)表示为____________。若制得这种锰锌铁氧体的质量为100 kg,在制取过程中不考虑损耗,需补充硫酸锰晶体(MnSO4·H2O)_________kg。(只列出计算式)