题目内容
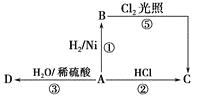
【题目】硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、漂白粉等一系列物质,转化关系如图所示。下列说法正确的是( )

A.CO、SO2、SO3均是酸性氧化物
B.除去与水的反应,图示转化反应均为氧化还原反应
C.工业上利用Cl2和石灰乳反应来制取漂白粉
D.用CO合成CH3OH进而合成HCHO的两步反应,原子利用率均为100%
【答案】BC
【解析】
A.CO与碱和水都不反应,是不成盐氧化物,不属于酸性氧化物,故A错误;
B.除去与水反应的两个反应,图示其余转化反应均有单质参加反应,元素的化合价一定发生变化,属于氧化还原反应,故B正确;
C.澄清石灰水的浓度较低,吸收效果差,为增强吸收效果,提高产率,工业用Cl2和石灰乳反应制取漂白粉,故C正确;
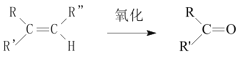
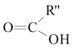
D.CH3OH发生催化氧化反应生成HCHO和H2O,原子利用率达不到100%,故D错误;
故选BC。

【题目】工业上用铝土矿(主要成分为Al2O3,含有少量SiO2、FeO·xFe2O3等杂质)制取铝的一种工艺流程示意图如下:
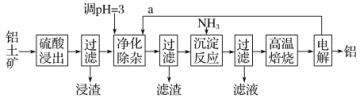
已知:生成氢氧化物沉淀的pH如下表。
沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
pH | 3.2 | 5.2 | 12.4 |
(1)为提高浸出速率,除适当增加硫酸浓度外,还可采取的措施有_______________
(2)浸渣的主要成分为____________________
(3)净化除杂操作分为两步:第一步是通入气体a,其目的是_____________________。第二步是控制溶液pH,只使Fe3+转化为Fe(OH)3沉淀。净化除杂生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是_____________________
(4)写出沉淀反应操作中发生反应的离子方程式:________________________。
(5)实验室高温焙烧时,用于盛放固体的仪器名称是_______________。
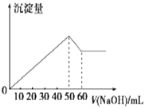
(6)在AlCl3和MgCl2的混合液中滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原溶液中AlCl3和MgCl2的物质的量之比为__________,并写出加入NaOH溶液的体积为50-60mL时的化学反应方程式__________________________。