题目内容
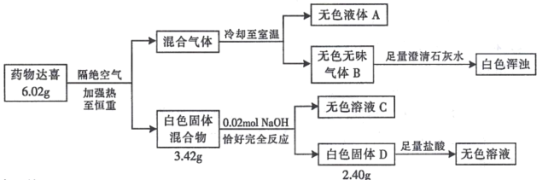
【题目】I.治疗胃酸过多的药物达喜(其式量不超过 700)由五种短周期元素组成,按如下流程进行实验以确定其组成。
请回答:
(1)达喜的化学式是_____________。
(2)达喜与胃酸(含稀盐酸)反应的化学方程式是____________。
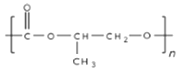
(3)气体 B 与环氧丙烷(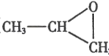 )可制得一种可降解高聚物,该反应的化学方程式是_____________________(有机物用结构简式表示)。
)可制得一种可降解高聚物,该反应的化学方程式是_____________________(有机物用结构简式表示)。
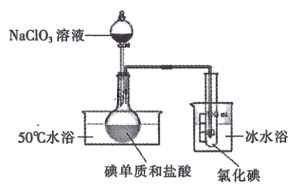
II.将 NaC1O3 溶液逐滴加入到碘单质和过量盐酸的混合液中可制备液态 ICl,实验装置如下图:
请回答:
(1)圆底烧瓶中发生的化学反应是______________( 用化学方程式表示)。
(2)若加入的 NaClO3 溶液已足量,请设计实验方案证明该反应已完全:_______。
【答案】Al2O36MgOCO212H2O或 2Al(OH)35Mg(OH)2MgCO34H2O或Al2Mg6(OH)16(CO3)4H2O Al2Mg6(OH)16(CO3)4H2O+18HCl=2AlCl3+ 6MgCl2+CO2↑+21H2O nCO2+n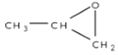
![]()
 3I2 +NaClO3+ 6HCl=6ICl + NaCl + 3H2O 取烧瓶内溶液,加淀粉溶液,如果不变蓝,说明反应已完全
3I2 +NaClO3+ 6HCl=6ICl + NaCl + 3H2O 取烧瓶内溶液,加淀粉溶液,如果不变蓝,说明反应已完全
【解析】
I.达喜隔绝空气加强热分解生成的气体冷却至室温,无色液体A是水,说明达喜中含有H和O。无色无味气体B通入足量石灰水产生白色沉淀,气体B是二氧化碳,说明达喜中含有C。达喜加热分解产生的固体中加入0.02molNaOH,不溶于NaOH溶液的2.40g白色固体D能溶于盐酸中,所以固体D是MgO,2.40gMgO为0.06mol。溶于NaOH溶液中的是Al2O3,其质量为3.42g-2.40g=1.02g,为0.01mol。所以达喜中含有的五种短周期元素为H、C、O、Mg、Al。
I.(1) 达喜中含有的五种短周期元素为H、C、O、Mg、Al,若以氧化物的形式表示,可以表示为:aMgObAl2O3cCO2dH2O。Al2O3为0.01mol,若b=1,则达喜的相对分子质量为6.02g÷0.01mol=602<700,所以可以确定达喜的相对分子质量为602。MgO为0.06mol,所以a=6。根据达喜的化学式和相对分子质量,有44c+18d=602-6×40-102=260,假设c=1,则d=12;假设c=2,d=9.6;假设c=3,d=7.1;假设c=4,d=4.7;假设c=5,d=2.2;d不是整数的都不符合题意,所以达喜的化学式为6MgOAl2O3CO212H2O,或表示为Al2O36MgOCO212H2O或2Al(OH)35Mg(OH)2MgCO34H2O或Al2Mg6(OH)16(CO3)4H2O。
(2)达喜与胃酸(含稀盐酸)反应,可以看做是碱或碱性氧化物和酸的反应,化学方程式是Al2Mg6(OH)16(CO3)4H2O+18HCl=2AlCl3+ 6MgCl2+CO2↑+21H2O。
(3)利用CO2中的一个碳氧双键与环氧丙烷(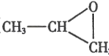 )发生加聚反应,得到聚酯类高聚物,酯在自然界中可以降解,该反应的化学方程式是nCO2+n
)发生加聚反应,得到聚酯类高聚物,酯在自然界中可以降解,该反应的化学方程式是nCO2+n
![]()
 。
。
II.(1) 将NaC1O3溶液逐滴加入到碘单质和过量盐酸的混合液中,生成ICl,氯的化合价从+5价降低到-1价,碘的化合价从0价升高到+1价,根据电子守恒和质量守恒配平得到化学方程式为:3I2 +NaClO3+ 6HCl=6ICl + NaCl + 3H2O。
(2)若加入的NaClO3 溶液已足量,则溶液中的碘全部被消耗,加入淀粉溶液时不变蓝。所以可以取烧瓶内溶液,加淀粉溶液,如果不变蓝,说明反应已完全。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案