题目内容
一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷
和氧气,其总反应为:2C2H6+702+8KOH=4K2C03+10H20,有关此电池的推断正确的
是( )。
和氧气,其总反应为:2C2H6+702+8KOH=4K2C03+10H20,有关此电池的推断正确的
是( )。
| A.负极反应为:14H20+702+28e-=280H- |
| B.放电一段时间后,负极周围pH升高 |
| C.每消耗1 mol C2H6,则电路上转移的电子为14 mol |
| D.放电过程中KOH的物质的量浓度不变 |
C
试题分析:该装置是燃料电池,乙烷失电子发生氧化反应,应为原电池负极,负极反应式为C2H6+18OH--14e-=2CO32-+12H2O,O2得电子被还原,应为原电池正极,电极反应式为2H2O+O2+4e-=4OH-,A选项错误,选项中给出的为正极反应。B选项错误,放电一段时间后正极周围PH升高。C选项争取。D选项错误,根据放映方程式可知,PH值降低。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
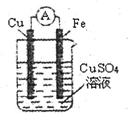
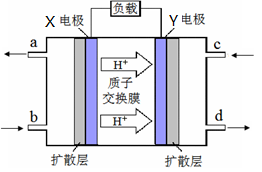
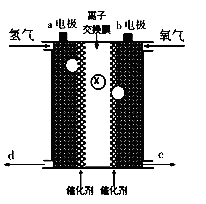
 ,
,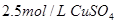 溶液,如有
溶液,如有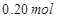 电子发生转移,试回答下列问题:
电子发生转移,试回答下列问题: 的质量是 ,得到
的质量是 ,得到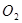 的体积(标准状况)是 。
的体积(标准状况)是 。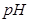 (填“变小”、“变大”或“不变”)
(填“变小”、“变大”或“不变”)