题目内容
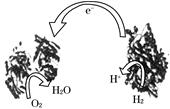
绿色电源“二甲醚-氧气燃料电池”的工作原理如下图所示下列说话正确的是:
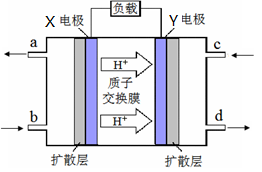

| A.氧气应从c处通入,电极Y上发生的反应为O2+4e-+2H2O==4OH- |
| B.电池在放电过程中,电极X周围溶液的pH增大 |
| C.二甲醚应从b处加入,电极X上发生的反应为(CH3)2O—12e-+3H2O=2CO2+12H+ |
| D.当该电池向外电路提供2mol电子时消耗O2约为11.2L |
C
A、氧气应从c处通入,C为正极,反应式为O2+4e-+4H+=2H2O,A错误;B.电池在放电过程中,二甲醚应从b处加入,电极X上发生的反应为(CH3)2O-12e-+3H2O=2CO2+12H+,电极X周围溶液的pH减小,B错误;C正确,D、O2没有指明状态,D错误,选C。

练习册系列答案
 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案
相关题目

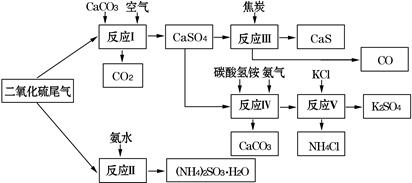
 CaS+4CO↑
CaS+4CO↑