题目内容
100毫升含HNO3、H2SO4的稀溶液中,加入9.6克铜充分反应,铜全溶,产生2.24升NO(标准状况)。同体积的混合酸恰好与250毫升2mol/L的NaOH完全中和。
计算原混合酸中HNO3的物质的量浓度的取值范围_________________________
H2SO4的物质的量浓度的取值范围_______________________。
1 mol/L≤C(HNO3)<5 mol/L, 0<C(H2SO4)≤2 mol/L
解析试题分析:本题用极限法考虑,铜与混酸反应的离子方程式为3Cu+2NO3-+8H+="3" Cu 2++2NO↑+4 H2O,2.24L标准状况下的NO的物质的量是0.1mol,若硝酸全部被还原为NO,则硝酸的物质的量最小是0.1mol,浓度是1mol/L;同体积的混合酸恰好与250毫升2mol/L的NaOH完全中和,说明混酸中的氢离子的物质的量为0.5mol,若全部是硝酸提供,则硝酸的物质的量最大是0.5mol,浓度是5mol/L,所以硝酸的物质的量浓度的范围是1 mol/L≤C(HNO3)<5 mol/L;当硝酸的物质的量最小时,硫酸的物质的量最大是0.2mol,所以浓度的最大值是2mol/L,硝酸物质的量最大时,硫酸的物质的量最小为0,实际是硝酸和硫酸的混合酸,所以硫酸的浓度的取值范围是 0<C(H2SO4)≤2 mol/L。
考点:考查金属与酸的计算,酸的浓度的计算

取等质量的钠进行下列实验,其中生成氢气最多的是
| A.将钠投入足量的水中 |
| B.将钠投入足量的稀硫酸中 |
| C.将钠用铝箔包好并刺一些小孔,再放入足量的水中 |
| D.将钠用耐热塑料薄膜包好并刺一些小孔,再放入足量的水中 |
(15分)用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/LFeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压值:)
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| I | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| II | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| III | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(2)I中,Fe2+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应的方程式_____。
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有_____性。
(4)II中虽未检测出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| IV | a>x≥c | 无明显变化 | 有Cl2 |
| V | c>x≥b | 无明显变化 | 无Cl2 |
②IV中检测Cl2的实验方法:____________________。
③与II对比,得出的结论(写出两点):___________________。

 2LiH Ⅱ.LiH+H2O=LiOH+H2↑
2LiH Ⅱ.LiH+H2O=LiOH+H2↑
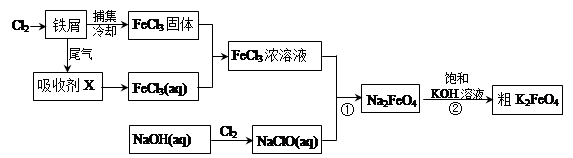
 K2FeO4+2NaOH,请根据相关反应原理分析反应能发生的原因 。
K2FeO4+2NaOH,请根据相关反应原理分析反应能发生的原因 。