题目内容
(8分)取100mL FeCl3、AlCl3的混合溶液,逐滴加入物质的量浓度为1 mol·L-1的NaOH溶液,生成沉淀的物质的量随加入NaOH溶液的体积(单位为mL)关系如下图所示。
按要求回答:
(1)a点对应沉淀的物质的量是 mol;此时溶液中的溶质是 。
(2)b点对应沉淀的物质的量是 mol;原溶液中c(AlCl3)= mol·L-1。
(8分,每空2分)
(1) 0.1; NaCl,
(2) 0.04; 0.6
解析试题分析:(1)a点对应沉淀是沉淀的最大量,根据元素守恒,氢氧化铁和氢氧化铝沉淀中氢氧根离子是沉淀物质的量的3倍,所以沉淀的物质的量是氢氧化钠物质的量的1/3,300mL的氢氧化钠的物质的量是0.3mol,所以a点对应沉淀的物质的量是0.1mol,此时溶液中的溶质是NaCl;
(2)b点对应沉淀是氢氧化铁沉淀,氢氧化铝沉淀与60mL的氢氧化钠溶液反应,根据Al(OH)3~OH-,判断氢氧化铝沉淀的物质的量是0.06L×1 mol·L-1=0.06mol,所以b点对应沉淀的物质的量是0.1mol-0.06mol=0.04mol;根据铝元素守恒,原溶液中n(AlCl3)=0.06mol,则c(AlCl3)=0.06mol/0.1L=0.6mol/L.。
考点:考查对图像的分析能力,氢氧化铝与氢氧化钠溶液的计算

利用下图装置做铝热反应实验。下列说法不正确的是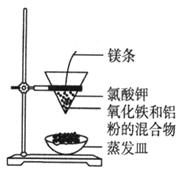
A.该反应的化学方程式是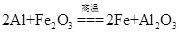 |
| B.该反应会产生高温、发出强光 |
| C.根据铝热反应的原理,可以冶炼某些金属 |
| D.若反应中转移3 mol电子,则消耗氧化剂的物质的量是1 mol |
王老师在用酒精喷灯做“铁与水蒸气反应”后,该校高一化学研究性小组同学对得到的黑色固体物质进行了如下实验:
(1)甲同学认为:该黑色固体为四氧化三铁。请写出黑色固体溶于稀盐酸的化学方程式____________;
(2)乙同学提出:根据上述实验现象甲同学的观点不可靠,理由是__________;
(3)深红色溶液C放置一段时间后,发现红色褪去。关于溶液褪色的原因,同学们纷纷猜想:
假设一:氯水有强氧化性,将溶液中的SCN—氧化;
假设二:空气中有还原性物质,将 ;
假设三:氯水有极强的氧化性,将 ;
基于假设一,为验证合理与否,可选用试剂:浓硫酸、1.0mol·L-1HNO3、1.0mol·L-1盐酸、1.0mol·L-1NaOH、0.lmol·L-1FeC13、0.lmol·L-1 CuSO4、20%KSCN、蒸馏水。
| 实验操作 | 预期现象 | 结论 |
| 取少量褪色后的溶液, | | 说明假设一是合理的 |
(4)乙同学用酒精灯加热做铁与水蒸气反应的实验,也得到了黑色固体,它不能被磁铁吸引,当加入盐酸溶解该固体时,溶液呈浅绿色,再滴加KSCN溶液不变色。由此她认为生成该固体的化学方程式为 。