题目内容
钢铁的锈蚀过程中,下列五种变化可能发生的是( )
①Fe由+2价转化为+3价 ②O2被还原 ③H+被还原 ④有Fe2O3?xH2O生成 ⑤杂质碳被氧化除去.
①Fe由+2价转化为+3价 ②O2被还原 ③H+被还原 ④有Fe2O3?xH2O生成 ⑤杂质碳被氧化除去.
| A、①② | B、③④ | C、①②③④ | D、①②③④⑤ |
分析:钢铁生锈的过程是金属铁发生了吸氧腐蚀的原电池原理,铁为负极,正极上是氧气得电子发生还原反应.
解答:解:中性电解质环境下,钢铁生锈的过程中的化学变化为:负极:Fe-2e-=Fe2+,正极:2H2O+O2+4e-=4OH-,总反应为:2Fe+2H2O+O2+4e-=2Fe(OH)2,Fe(OH)2迅速被氧化:4Fe(OH)2+O2+2H2O=4Fe(OH)3,Fe(OH)3失水变成Fe2O3?3H2O,酸性电解质环境下,钢铁生锈的过程中的化学变化为:负极:Fe-2e-=Fe2+,正极:2H++2e-=H2↑,总反应为Fe+2H+=2Fe2++H2↑.
故选C.
故选C.
点评:金属的吸氧腐蚀是较为普遍的金属腐蚀方式,可以根据所学的原电池原理知识来回答,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
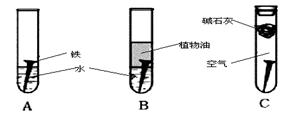
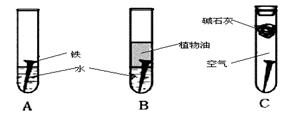
全世界每年因钢铁锈蚀造成大量的损失.某学生欲探究在蒸馏水、氯化钠溶液和醋酸溶液三种条件下铁锈蚀的快慢,设计了如下实验.
请回答:
(1)在一周的观察过程中,他发现实验序号为 的试管中铁钉锈蚀速度最慢.
(2)实验②中发生的是 (填“电化学腐蚀”或“化学腐蚀”).
(3)下列防止钢铁锈蚀的措施合理的是 (填字母).
a.在自行车的钢圈表面镀镍
b.在地下钢铁管道上连接铜块
c.改变金属内部结构制成不锈钢
(4)已知铁钉样品质量为4.00g,经实验测得未锈蚀铁的质量分数为70%.则未锈蚀铁与足量稀硫酸反应生成氢气的体积为 (标准状况).
| 实验序号 | ① | ② | ③ |
| 实验 内容 |
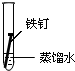 |
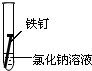 |
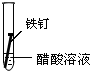 |
(1)在一周的观察过程中,他发现实验序号为
(2)实验②中发生的是
(3)下列防止钢铁锈蚀的措施合理的是
a.在自行车的钢圈表面镀镍
b.在地下钢铁管道上连接铜块
c.改变金属内部结构制成不锈钢
(4)已知铁钉样品质量为4.00g,经实验测得未锈蚀铁的质量分数为70%.则未锈蚀铁与足量稀硫酸反应生成氢气的体积为