题目内容
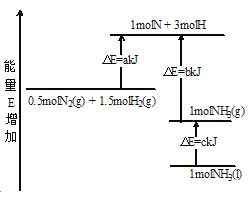
【题目】化学反应N2+3H2![]() 2NH3的能量变化如图所示,该反应的热化学方程式是
2NH3的能量变化如图所示,该反应的热化学方程式是
A. N2(g)+3H2(g)![]() 2NH3(l) △H= 2(a﹣b﹣c)kJ/mol
2NH3(l) △H= 2(a﹣b﹣c)kJ/mol
B. N2(g)+3H2(g)![]() 2NH3(g)△H=2(b﹣a)kJ/mol
2NH3(g)△H=2(b﹣a)kJ/mol
C. 0.5N2(g)+1.5H2(g)![]() NH3(l)△H=(b+c﹣a)kJ/mol
NH3(l)△H=(b+c﹣a)kJ/mol
D. 0.5N2(g)+1.5H2(g)![]() NH3(g)△H=(a+b)kJ/mol
NH3(g)△H=(a+b)kJ/mol
【答案】A
【解析】
由图可以看出,△E为反应的活化能,反应热等于反应物的活化能减生成物的活化能,所以1/2N2(g)+3/2H2(g)=NH3(g)△H=(a-b)kJ/mol,即N2(g)+3H2(g)2NH3(g)△H=-2(b-a) kJ/mol,而1mol的NH3(g)转化为1mol的NH3(l)放出的热量为ckJ,根据盖斯定律有:1/2N2(g)+3/2H2(g)=NH3(l)△H=(a-b-c)kJ/mol,即:N2(g)+3H2(g)2NH3(1)△H=2(a-b-c)kJmol-1,故A正确;故选A。

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目