题目内容
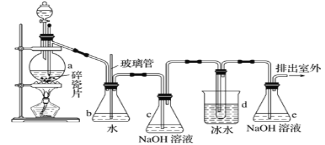
【题目】1,2-二溴乙烷可作抗爆剂的添加剂。如图为实验室制备1,2-二溴乙烷的装罝图,图中分液漏斗和烧瓶a中分别装有浓H2SO4和无水乙醇,d装罝试管中装有液溴。
相关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
密度/g·cm-3 | 0.79 | 2.18 | 0.71 | 3.10 |
沸点/℃ | 78.5 | 131.4 | 34.6 | 58.8 |
熔点/℃ | -114.3 | 9.79 | - 116.2 | -7.2 |
水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(1)装置a中发生主要反应的方程式为:___。为防止副反应发生,实验中的具体操作为:___。
(2)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装罝中导管是否发生堵塞,如果实验时d装罝中导管堵塞,你认为可能的原因:___;安全瓶b还可以起到的作用是:___。
(3)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是___。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比理论值超过许多,如果装罝的气密性没有问题,试分析可能的原因:___、___(写出两条即可)。
【答案】CH3-CH2-OH ![]() CH2=CH2↑+H2O 将温度迅速升高到170℃ 过度冷却,产品1,2-二溴乙烷在装罝d中凝固 防止倒吸 吸收乙烯气体中含有的CO2、SO2等酸性气体 浓硫酸将部分乙醇氧化;发生副反应生成乙醚; 乙醇挥发;乙烯流速过快,未完全发生加成反应
CH2=CH2↑+H2O 将温度迅速升高到170℃ 过度冷却,产品1,2-二溴乙烷在装罝d中凝固 防止倒吸 吸收乙烯气体中含有的CO2、SO2等酸性气体 浓硫酸将部分乙醇氧化;发生副反应生成乙醚; 乙醇挥发;乙烯流速过快,未完全发生加成反应
【解析】
(1)根据乙烯能和溴水反应生成1,2-二溴乙烷分析,装置中先制取乙烯气体,据此书写方程式。
(2)根据反应过程中可能存在的副反应分析实验的注意事项。
(3)根据乙烯气体中可能的杂质气体为二氧化碳和二氧化硫等分析氢氧化钠的作用。
(4)根据浓硫酸具有强氧化性和乙醇具有挥发性等分析。
(1) 装置a中为乙醇在浓硫酸条件下反应生成乙烯,方程式为:CH3-CH2-OH ![]() CH2=CH2↑+H2O,因为乙醇加热到140度时可以反应生成乙醚,所以为了防止副反应发生,实验中具体操作为将温度迅速升高到170℃;
CH2=CH2↑+H2O,因为乙醇加热到140度时可以反应生成乙醚,所以为了防止副反应发生,实验中具体操作为将温度迅速升高到170℃;
(3)装置d中发生堵塞,可能是因为过度冷却,产品1,2-二溴乙烷在装罝d中凝固;后面的液体可能倒吸到安全瓶b中,但不可能倒吸回反应装置中,所以可以防止倒吸;
(4)氢氧化钠能吸收二氧化碳或二氧化硫等酸性气体,故其作用为:吸收乙烯气体中含有的CO2、SO2等酸性气体;
(5)反应过程中浓硫酸具有强氧化性,可能将部分乙醇氧化;或因为温度控制不当,发生副反应生成乙醚;或因为乙醇挥发造成产物量减少;或因为乙烯流速过快,未完全发生加成反应。

 通城学典默写能手系列答案
通城学典默写能手系列答案【题目】下列有关实验现象和解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 向淀粉的酸性水解液中滴入少量新制Cu(OH)2悬浊液并加热 | 有砖红色沉淀生成 | 葡萄糖具有还原性 |
B | NaAlO2溶液与NaHCO3溶液混合 | 白色絮状沉淀生成 | 二者水解相互促进生成氢氧化铝沉淀 |
C | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2 的△H<0 |
D | 向盛有1mL0.l mol/L的AgNO3溶液中加入10滴0.1mol/L的NaCl溶液,振荡,再加入10滴0.1mol/L的NaI溶液,再振荡 | 先生成白色沉淀,后产生黄色沉淀 | Ksp(AgI)sp(AgCl) |
A. A B. B C. C D. D






