题目内容
【题目】硫酸亚铁铵又称莫尔盐,是浅绿色晶体.它在空气中比一般亚铁盐稳定,是常用的Fe2+试剂.某实验小组利用工业废铁屑制取莫尔盐,并测定其纯度.
已知:①
| 10 | 20 | 30 | 40 | 50 | 70 |
(NH4)2SO4 | 73.3 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
FeSO47H2O | 40.0 | 48.0 | 60.0 | 73.3 | ﹣ | ﹣ |
(NH4)2SO4FeSO46H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
②莫尔盐在乙醇溶剂中难溶.
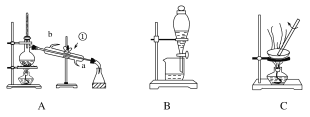
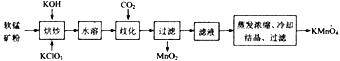
Ⅰ.莫尔盐的制取

试分析:
(1)必须在铁屑少量剩余时进行过滤,其原因是______________________.
(2)步骤3中包含的实验操作名称_____________________.
(3)产品莫尔盐最后用______________________ 洗涤(填字母编号).
a.蒸馏水 b.乙醇 c.滤液
Ⅱ.为测定硫酸亚铁铵(NH4)2SO4FeSO46H2O晶体纯度,某学生取m g硫酸亚铁铵样品配制成500mL溶液。根据物质组成甲、乙、丙三位同学设计了如下三个实验方案,请回答:
方案一:取20.00mL硫酸亚铁铵溶液用0.1000molL﹣1的酸性KMnO4溶液分三次进行滴定.
方案二:取20.00mL硫酸亚铁铵溶液进行如下实验.
![]()
(4)若实验操作都正确,但方案一的测定结果总是小于方案二,其可能原因为_________,验证推测的方法为:___________________________________________方案三:(通过NH4+测定)实验设计图如下所示.取20.00mL硫酸亚铁铵溶液进行该实验.

(5)装置___________ (填“甲”或“乙”)较为合理,判断理由是_______________.
(6)量气管中最佳试剂是__________ (填字母编号.如选“乙”则填此空,如选“甲”此空可不填).
a.水 b.饱和NaHCO3溶液 c.CCl4
(7)若测得NH3的体积为V L(已折算为标准状况下),则该硫酸亚铁铵晶体的纯度为_______.
【答案】 防止亚铁离子被氧化为三价铁离子 加热浓缩、降温结晶 b 硫酸亚铁铵溶液在空气中亚铁离子被氧化 取硫酸亚铁铵溶液向其中滴入KSCN溶液,若变成红色则推测成立 乙 甲装置容易引发倒吸 c 392V×25/44.8m ×100%
【解析】试题分析:(1). 铁具有还原性,能防止亚铁离子被氧化;(2)硫酸亚铁铵在低温时溶解度小;莫尔盐难溶于乙醇;(4)在空气中亚铁离子被氧化;三价铁离子遇KSCN溶液变为血红色;(5)甲装置易引起倒吸;(6)氨气易溶于水,不溶于四氯化碳;(7)根据关系式![]() 计算纯度;
计算纯度;
解析:(1). 铁具有还原性,能防止亚铁离子被氧化为三价铁离子,所以在铁屑少量剩余时进行过滤;(2)硫酸亚铁铵在低温时溶解度小,所以步骤3中获得硫酸亚铁铵包含的实验操作名称加热浓缩、降温结晶;(3)莫尔盐难溶于乙醇,所以最后用乙醇洗涤,故选b;(4)在空气中亚铁离子被氧化,所以案一的测定结果总是小于方案二,其可能原因为硫酸亚铁铵溶液在空气中亚铁离子被氧化;三价铁离子遇KSCN溶液变为血红色,检验亚铁离子被氧化的方法是取硫酸亚铁铵溶液向其中滴入KSCN溶液,若变成红色则推测成立;(5)甲装置易引起倒吸,所以装置乙合理;(6)氨气易溶于水,不溶于四氯化碳,所以量气管中最佳试剂是CCl4,选c;(7)设每次滴定液中含有晶体的质量为xg;
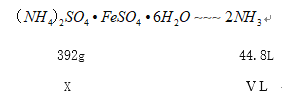
![]()
X=![]() ,该硫酸亚铁铵晶体的纯度为
,该硫酸亚铁铵晶体的纯度为![]() 。
。